在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图: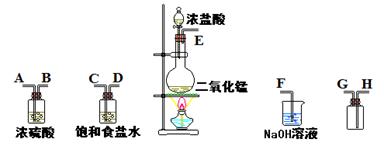
(1)连接上述仪器的正确顺序(填各接口处的字母): 接 ; 接 ;
接 ; 接 。
(2)装置中,饱和食盐水的作用是 ;NaOH溶液的作用是 。
(3)化学实验中常用湿润的淀粉—KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到 ,反应方程式 。
(4)写出下列化学反应的方程式:
①气体发生装置中进行的反应:
②NaOH溶液中发生的反应:
(5)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O。
①标出该反应电子转移的方向和数目
②氧化剂和还原剂的物质的量之比为 ;
③当有0.2mole-转移时被氧化的HCl的质量是 ;该反应中被氧化和未被氧化的盐酸的物质的量之比是 ,
④如果将20ml 12mol·L-1的浓盐酸与足量KMnO4充分反应,实际能收集到的氯气在标准状况下的体积将 。
| A.≥1.68L | B.>1.68L | C.≤1.68L | D.<1.68L |
化合物A、D、F是中学化学中最常见的物质,化合物B、C、E中含有两种相同的元素,这些化合物之间存在如下关系。其中A和B的反应是一种重要化工生产中的主要反应。
据此推断:
(1)在A、C、F中含有的相同元素是 。
(2)化合物C的化学式为 。
(3)A和B反应的化学方程式为 ,
该反应是在 中进行的(填设备名称)。
(4)C的水溶液和D能否发生反应? 。其理由是 。
若能够反应,则该反应的离子方程式为 (若不能,则此空不填)。
铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中表现出的性质是_____,该反应的还原产物是_____。
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是_____,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是_____mol。
(3)0.3molCu被另一浓度的硝酸完全溶解后,如果此时产生的NO和NO2气体总体积在标准状况下为8.96 L,则被还原的硝酸的物质的量是_____mol,参加反应的硝酸的物质的量是_____mol,产生的混合气体中NO和NO2体积比为_______。
用于分离或提纯物质的方法有:
| A.蒸馏(分馏) |
| B.萃取 |
| C.过滤 |
| D.重结晶 |
E.分液。
下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号.)
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒()
(2)分离四氯化碳与水的混合物()
(3)分离汽油和煤油()
(4)分离碘水中的碘单质()
(5)提纯氯化钠和硝酸钾混合物中的硝酸钾()
将0.1 mol的镁和铝的混合物溶于50 mL 4 mol·L-1H2SO4溶液中,然后再滴加2 mol·L-1的NaOH溶液。请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V的变化如图所示。当V1=80 mL时,计算金属粉末中镁的物质的量及V2的体积。
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,计算滴入NaOH溶液的体积。
含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)在元素周期表中,A位于 族,与A同族但相对原子质量比A小的元素B的原子结构示意图为 ,A与B在原子的电子层结构上的相同点是 。
(2)易与C发生化学反应的酸是 ,反应的化学方程式是 。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①写出生成D和F的化学反应方程式: 。
②要将纯碱高温熔化,下列坩埚中可选用的是 。
A.普通玻璃坩埚B.石英玻璃坩埚
C.氧化铝坩锅D.铁坩锅
(4)100gC与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是 。