过碳酸钠(Na2CO3·3H2O2),有固体双氧水的俗称,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,过碳酸钠的某生产流程如下图所示。已知:2Na2CO3+3H2O2=2Na2CO3·3H2O2 △H<0;回答下列问题: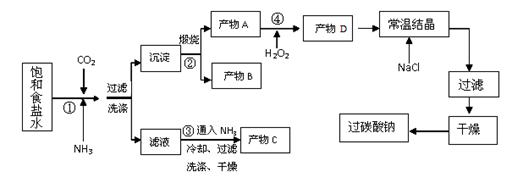
(1)下列物质可使过碳酸钠较快失效的是(填序号) 。
| A.FeCl3溶液 | B.H2S | C.稀硫酸 | D.NaHCO3溶液 |
(2)已知产物C是一种常用氮肥,则其化学式为 ,
反应①的总反应方程式为 。
(3)该生产流程中可循环使用的物质是 。
(4)生产过碳酸钠的流程中遗漏了一步,造成所得产品纯度偏低,该步操作的名称是 。
通常羟基与烯键碳原子相连接时,易发生下列转化:
现有下图所示的转化关系:
已知E能溶于NaOH溶液中,F转化为G时,产物只有一种结构,且能使溴水褪色。请回答下列问题:
(1)结构简式:A_____;B______。
(2)C→D的化学方程式:______。
F→G的化学方程式:______。
实验室里有一瓶KCl与CaCl2的固体混合物,通过下面实验可确定该混合物中KCl和CaCl2的质量比,也可制得纯净的KCl,根据实验步骤填写下列空白:
(1)调整零点时,若指针偏向左边,应将左边的螺丝帽向(填左、右)______旋动。
(2)某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如图3-2示。
下面的操作应该是_______和______。
(3)加入的A是______,检验A是否过量的方法是______。

(4)过滤时,某学生的操作如图3-3所示,用文字说明图中的错误_____。
(5)滤液中加入的B物质是_______,应该加入过量B物质,理由是_____。
(6)为检验沉淀是否洗净,应在最后几滴洗出液中加入______,若______,表示沉淀已洗净。
(7)得到的固体C是_______。
(8)该混合物中KCl和CaCl2质量比的计算式是_____。
(9)配制100mL0.20mol·L-1的KCl溶液:某学生将准确称取的1.49gKCl固体放入烧杯中,加入约30mL蒸馏水,用玻璃棒搅拌使其溶解,将溶液由烧杯转移到100mL容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近标线2—3cm处,改用胶头滴管加蒸馏水,使溶液凹面最低点恰好与刻度相切,把容量瓶盖盖好,振荡摇匀,该学生操作中错误的是_____。
2008年9月,三聚氰胺污染牛奶事件,在社会上造成了很坏的影响。牛奶和奶粉中添加三聚氰胺,主要是因为它能冒充蛋白质。已知三聚氰胺中含有碳、氢、氮三种元素,其相对分子质量为126,为测定三聚氰胺的组成,用下列各仪器装置,再过量的氧气流中将2.52g三聚氰胺样品氧化成CO2、H2O和N2。回答下列问题:

 (1)产生的氧气按从左向右流向,所选装置的连接顺序为:
(1)产生的氧气按从左向右流向,所选装置的连接顺序为: D接、、、、。
D接、、、、。 (2)装置C的作用是,装置F中CuO的作用是;装置D中发生的反应化学方程式是。
(2)装置C的作用是,装置F中CuO的作用是;装置D中发生的反应化学方程式是。 (3)实验后称得A、B两装置的质量分别增加2.64g和1.08g,则三聚氰胺分子中碳、氢、氮的原子个数比为
(3)实验后称得A、B两装置的质量分别增加2.64g和1.08g,则三聚氰胺分子中碳、氢、氮的原子个数比为 (4)目前较多采用以尿素为原料,在0.1MPa下,390℃左右时,以硅胶做催化剂合成三聚氰胺。反应过程中,除生成CO2外,还生成一种使湿润的红色石蕊试纸变蓝的气体,试写出制备三聚氰胺的化学方程式(有机物可用分子式)
(4)目前较多采用以尿素为原料,在0.1MPa下,390℃左右时,以硅胶做催化剂合成三聚氰胺。反应过程中,除生成CO2外,还生成一种使湿润的红色石蕊试纸变蓝的气体,试写出制备三聚氰胺的化学方程式(有机物可用分子式) (5)按(1)的连接方法,此实验装置存在的缺陷是
(5)按(1)的连接方法,此实验装置存在的缺陷是
夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣。璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应。鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色。下图是北京鸟巢试放烟火奥运五环图,并回答下列问题:

 ⑴火焰利用了部分金属的元素特征的反应,该反应属于(填“物理”或“化学”变化。
⑴火焰利用了部分金属的元素特征的反应,该反应属于(填“物理”或“化学”变化。 ⑵ 现在有一种火焰的引发是当浓H2SO4滴下去跟氯酸钾起作用时,便生成了奇臭的二氧化氯气体且发现只有氯元素的化合价发生变化。请写出该反应的方程式
⑵ 现在有一种火焰的引发是当浓H2SO4滴下去跟氯酸钾起作用时,便生成了奇臭的二氧化氯气体且发现只有氯元素的化合价发生变化。请写出该反应的方程式 ⑶下图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为
⑶下图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C、D均为原子晶体,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:
,C、D均为原子晶体,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2。根据以上信息回答下列问题:

 ①B的水溶液呈弱酸性,其主要的电离方程式可表示为_______________________,D的化学式是_________.
①B的水溶液呈弱酸性,其主要的电离方程式可表示为_______________________,D的化学式是_________. ②A、B、E中均含有的一种元素符号为______________。
②A、B、E中均含有的一种元素符号为______________。 ③C与纯碱反应的化学方程式为____________________。
③C与纯碱反应的化学方程式为____________________。 ④液态B与液态E反应可生成一种单质和一种常见液体,1molB参加反应放出热量QkJ,其反应的热化学方程式为_______________________。
④液态B与液态E反应可生成一种单质和一种常见液体,1molB参加反应放出热量QkJ,其反应的热化学方程式为_______________________。
新华网2月22日电 截至22日15时,山西屯兰煤矿事故已造成73人遇难。据事故抢险指挥部介绍,现已初步查明,事故原因为井下局部瓦斯爆炸。该矿发生事故时井下共有矿工436人,有375人陆续升井。升井后经抢救无效死亡的和井下已发现遇难遗体的矿工共计73人。现有113人住院观察,其中21人伤势较重。目前,山西仍在全力搜救被困者,第一轮搜救已于14时结束,目前第二轮搜救排查已经展开,同时山西省还采取措施防止次生灾害发生。煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷。 ⑴下列关于甲烷的叙述中错误的是()
⑴下列关于甲烷的叙述中错误的是() A.甲烷分子是一种呈正四面体型的、含极性键的非极性分子
A.甲烷分子是一种呈正四面体型的、含极性键的非极性分子 B.甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子
B.甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 C.甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业
C.甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 D.“抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸
D.“抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 ⑵已知某正四面体形分子E和直线形分子G在光照条件下反应,生成一种直线形分子M和变形的四面体L(组成E.G.L.M分子的元素原子序数均小于18),且G分子中的原子处于E分子最大原子的下一周期。反应过程图示如下:
⑵已知某正四面体形分子E和直线形分子G在光照条件下反应,生成一种直线形分子M和变形的四面体L(组成E.G.L.M分子的元素原子序数均小于18),且G分子中的原子处于E分子最大原子的下一周期。反应过程图示如下:

 利用E与G发生取代反应制取副产品M溶液的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:
利用E与G发生取代反应制取副产品M溶液的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:


根据要求填空: ①B装置有三种功能:①控制气流速度;②均匀混合气体;③
①B装置有三种功能:①控制气流速度;②均匀混合气体;③ ②设V(G)/V(E)=x,若理论上欲获得最多的M,则x值应
②设V(G)/V(E)=x,若理论上欲获得最多的M,则x值应 ③D装置的石棉中均匀混有KI粉末,其作用是。
③D装置的石棉中均匀混有KI粉末,其作用是。 ④E装置的作用是(填编号)
④E装置的作用是(填编号) A.收集气体 B.吸收G物质 C.防止倒吸 D.吸收M物质
A.收集气体 B.吸收G物质 C.防止倒吸 D.吸收M物质 ⑤在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式。
⑤在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式。 ⑥E装置出生成盐酸外,还含有有机物,从E中分离出M的最佳方法为。
⑥E装置出生成盐酸外,还含有有机物,从E中分离出M的最佳方法为。 该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为
该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为