(6分)认识燃烧,科学地利用燃烧,使燃烧为人类服务是十分重要的。
为验证可燃物燃烧的条件,某兴趣小组进行了如下探究活动。
[查阅资料]白磷的着火点是40℃,红磷的着火点是240℃,两种物质的燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,能与空气中的水蒸气反应,生成有毒的偏磷酸(HPO3)。
[设计实验]小组同学设计了下图的实验装置进行实验。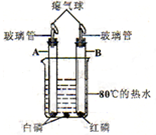
[收集证据]实验中获得了如下实验事实:
①A试管内的白磷燃烧;②热水中的白磷不燃烧;③B试管内的红磷不燃烧。
[得出结论]结论1:依据上述实验事实 (选填序号)可知:可燃物燃烧需与氧气接触。
结论2:依据上述实验事实①③可知:可燃物燃烧需满足的条件是 。
[拓展延伸]若将A试管上带玻璃管的橡皮塞换成实心橡皮塞,在实验中可能会发生的问题是: ;若去除A试管上带玻璃管的橡皮塞,在实验中又可能会出现的问题是: 。
[知识运用]我国的成语蕴含着丰富的化学知识。下面是一些与燃烧有关的成语的文学解释,请根据燃烧的条件和灭火的原理解释以下成语的化学含义。
煽风点火:比喻煽动别人闹事。 ;
釜底抽薪:抽去锅底下的柴火,比喻从根本上解决问题。 。
实验室获取氮气有很多种途径,常见的有3种方法。
方法一:将氨气(NH3)通过赤热的装有氧化铜的玻璃管,生成铜、氮气和水蒸气,除去水蒸气后测得氮气的密度为1.2508g/L。
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末,测得该气体的密度为1.2572g/L。 进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置)。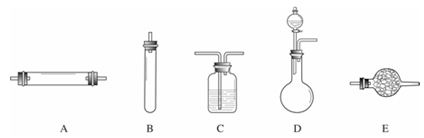
为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置(选填装置编号)中加入(填名称)以除去其它杂质气体。
方法三:将亚硝酸钠(NaNO2)和氯化铵的饱和溶液加热,氮元素全部转化为氮气。下图是实验室用这种方法制N2,并测定生成N2体积的装置(部分装置略去),请回答相关问题。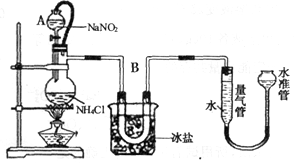
【查阅资料】
(1)NaNO2+NH4Cl NaCl+N2↑+2H2O(此反应会放出大量的热);
NaCl+N2↑+2H2O(此反应会放出大量的热);
(2)B部分中冰盐是冷凝作用
【实验探究】
①;
②20℃时,取含溶质0.21g饱和NH4Cl溶液放入烧瓶,连接装置;
③调节水准管,使其与量气管中液面相平,记录量气管中水面读数为12.0mL;
④打开分液漏斗活塞,逐滴滴入饱和NaNO2溶液,加热至反应发生,移走酒精灯;
⑤烧瓶中不再产生气泡时,关闭活塞;
⑥待冷却至室温,调节两边液面高度相平,记录量气管中水面读数为100.0mL;
⑦处理剩余药品,整理实验台。
【实验分析及数据处理】
(1)加入药品前必须进行的实验①是;
(2)步骤④中,移走酒精灯的目的是;
(3)计算生成氮气的质量和密度。(4分,计算过程中以及最终数据均保留2位小数)
【解释与结论】
1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比其他方法得到的纯氮气密度总是偏大5‰左右。若实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因
是(已知:相同条件下,气体的相对分子质量越大,密度就越大)
【反思与评价】
(1)装置中A部分的分液漏斗与蒸馏瓶之间连接的导管所起的作用是
A.防止NaNO2饱和溶液蒸发 B.保证实验装置不漏气
C.使NaNO2饱和溶液顺利滴下 D.防止溶液冲入U形管
(2)科学家瑞利仅仅是从小数点第三位数的差别,发现了新物质。这启示我们在今后的学习和生活中要学习科学家的.
A.严谨求实的科学态度和敢于怀疑的批判精神
B.科学研究中遇到疑惑就趁早放弃,不要浪费时间
C.不能因为微小的差异而放过一次成功的机会
D.要相信权威,权威一定是正确的
某牌子月饼盒内有一个小纸袋,上面写着“脱氧剂”,它的作用是除去袋内氧气,达到食品保鲜的目的。有三位同学打开小纸袋,看到“脱氧剂”大部分是灰黑色粉末,其中混有少量的红色粉末。
【提出问题】该“脱氧剂”中的灰黑色、红色粉末各是什么?
【猜想】甲同学认为灰黑色粉末为CuO、红色粉末为Cu
乙同学认为灰黑色粉末为Fe粉、红色粉末为Fe2O3
丙同学认为灰黑色粉末为C粉、红色粉末为Fe2O3
【设计方案】验证乙同学猜想的实验方案如下:
(1)请你参照上图的形式,将验证甲同学猜想的实验过程表示在下列图框中。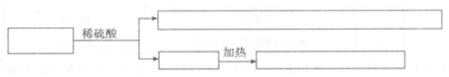
(2)你认为__________同学的猜想较合理,理由是_____________________________。
(3)请推测此“脱氧剂”除去氧气的反应原理,用化学方程式表示为_______________。
实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组发现一瓶未密闭的NaOH固体,对其成分提出以下假设,并完成了实验探究。
假设1:只含NaOH;
假设2:含NaOH和Na2CO3;
假设3:只含Na2CO3
(1)成分中可能含有Na2CO3的原因是(用化学方程式回答)。
(2)取少量样品于试管中,加入足量稀盐酸,观察到________________,说明假设2或假设3成立。
(3)进一步探究的过程如下: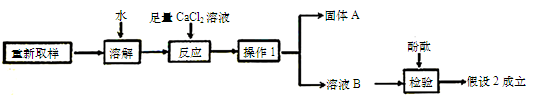
①“操作1”的名称是,
②“固体A”的化学式是___________。
③加入足量CaCl2溶液的作用是。
④溶液B中滴加酚酞后,观察到,说明假设2成立。
灰某兴趣小组对“蜡烛燃烧的产物”进行探究。
【查阅资料】蜡烛的主要成分是石蜡,石蜡由碳、氢两种元素组成。
【作出猜想】蜡烛燃烧的产物是二氧化碳和水。
【实验验证】(1)用干冷的小烧杯罩在蜡烛火焰上,观察到,证明有水生成。
(2)用涂有饱和石灰水的小烧杯罩在蜡烛火焰上,石灰水变浑浊,证明有二氧化碳生成。二氧化碳和石灰水反应的化学方程式为。
小明提出质疑:石灰水变浑浊不一定是生成碳酸钙,还可能是饱和石灰水受热后,析出了氢氧化钙。同学们又用右上图所示的装置进行实验,1分钟后,提起锥形瓶,翻转后注入20mL饱和石灰水,加塞、振荡,观察到石灰水变浑浊,确定有二氧化碳生成。
实验中小明观察到一个意外现象:锥形瓶内壁上有少量黑色物质。
【交流讨论】经分析,同学们一致认为黑色物质是石蜡不充分燃烧生成的。由此他们猜想还可能生成一氧化碳。
为验证一氧化碳,他们设计了如下图所示的实验。
【实验验证】(1)实验前,先在玻璃管的中部放入一团棉花,其目的是。
(2)将a端插入蜡烛的焰心。
(3)用酒精灯加热b端的氧化铜与水调和的糊状物,一段时间后,观察到黑色物质变成红色,证明蜡烛不充分燃烧有一氧化碳生成。
(4)为防止玻璃管中的红色物质又被氧化变成黑色,接下来的操作是:。
【拓展应用】含碳燃料不充分燃烧会生成一氧化碳等物质,浪费资源,且污染空气。为使其充分燃烧,应采取的措施是(答一条即可)。
某化学兴趣小组的四位同学对氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分进行了探究。
【作出猜想】小马猜想:溶质有NaCl、HCl、NaOH。
小程猜想:溶质只有NaCl
小宫猜想:溶质有NaCl、HCl
小尚猜想:溶质有NaCl、NaOH
(1)老师认为小马的猜想是错误的,其理由是_______________________________
【方案设计】小程和小宫分别设计如下方案验证各自的猜想。
| 方案设计者 |
方案步骤 |
方案预估现象 |
方案结论 |
| 小程 |
用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,把试纸所呈现的颜色与标准比色卡进行对照 |
pH=7 |
小程猜想正确 |
| 小宫 |
取少量反应后的溶液于一支试管中,再向试管中滴加稀硝酸和硝酸银溶液 |
有白色沉淀生成 |
小宫猜想正确 |
(2)两位同学中________________的方案正确。
【方案反思】
(3)请分析错误方案的原因:__________________________(若都正确,不作答)。
【拓展研究】
(4)请你再设计一个实验方案验证小尚的猜想正确,填写下列实验报告。
| 方案步骤 |
方案现象 |
方案结论 |
| 取少量反应后的溶液于一支试管中,再向试管中滴加________ 溶液 |
出现蓝色沉淀 |
小尚猜想正确 |