已知化学反应①:Fe(s)+CO2(g)=FeO(s)+CO(g),其平衡常数为K1;
化学反应②:Fe(s)+H2O(g)=FeO(s)+H2(g),其平衡常数K2。
在温度973 K和1173 K情况下,K1、K2的值分别如下:
| 温度 |
K1 |
K2 |
| 973 K |
1.47 |
2.38 |
| 1173 K |
2.15 |
1.67 |
(1)通常表格中的数值可以推断:反应①是____________(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)=CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=____________。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式____________。据此关系式及上表数据,也能推断出反应③是____________(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有____________(填写序号)。
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的浓度
一个体重50 kg的健康人身体中含铁2 g。铁在人体中不是以游离态的形式存在,而是以Fe2+和Fe3+形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的盐,如硫酸亚铁(FeSO4)。人体中经常进行Fe2+和Fe3+的转化,服用维生素C,可使食物中的Fe3+转化为Fe2+”,说明维生素C具有性。
(2)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是。
某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,
已知:As是产物之一。
(1)写出并配平该反应的化学方程式 ______________
(2)在反应中,每转移1 mol电子,消耗(或生成)HCl_______mol;
(3)下列叙述正确的是_____________(填写序号)。
a.在相同条件下,第VIIA族元素的阴离子的还原性从上到下逐渐增强
b.Sn和Pb位于同一主族,其+4价的化合物均很稳定
c.在相同条件下,还原性顺序:S2->I->Fe2+>Br->Cl-
d.在上述反应中,氧化性:SnCl2>As,还原性:H3AsO3>H2SnCl6
复分解反应是中学化学中常见的一种反应类型。
(1)已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH值:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
复分解存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3===2CH3COONa+CO2↑+H2O若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该 规律,请判断下列反应不能成立的是______(填编号)。
规律,请判断下列反应不能成立的是______(填编号)。
A、CO2+H2O +2NaClO===Na2CO3+2HClO
B、 CO2+H2O +NaClO===NaHCO3+HClO
CO2+H2O +NaClO===NaHCO3+HClO
C、CO2 +H2O +C6H5ONa NaHCO3+C6H5OH
NaHCO3+C6H5OH
D、CO2 +H2O +2C6H5ONa Na2CO
Na2CO 3+2C6H5OH
3+2C6H5OH
E、Na2CO3+C6H5OH NaHCO3+C6H5ONa
NaHCO3+C6H5ONa
F、CH3COOH+NaCN===CH3COONa+HCN
(2)根据前述信息判断,浓度均为0.05 mol/L的下列六种物质的溶液中,pH最小的是______(填编号); pH最大的是_________(填编号)。
pH最大的是_________(填编号)。
①C6H5OH ②CH3COOH ③HCN ④HClO ⑤H2 SO4 ⑥HClO4
SO4 ⑥HClO4
(3)一些复分解反应的发生还遵循其它的规律。下列转化都属于复分解反应:
①蒸发KCl和NaNO3混合溶液,首先析出NaCl晶体
②侯氏制碱法中,向饱和食盐水先通入足量氨气,再通入二氧化碳,可获得小苏打晶体
根据上述反应,总结出复分解反应发生的另一规律:______________;
将KI溶液和AgCl固体混合搅拌,会观察到 的现象是_______________,请写出反应的离子方程式: __________。
的现象是_______________,请写出反应的离子方程式: __________。
已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNa HSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示。
HSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示。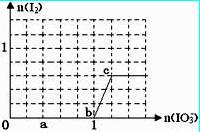
试回答下列问题:
(1)写出a点反应的离子方程式_____。
(2)写出b点到c点反应的离子方程式_________。
(3)当溶液中的I-为0.4 mol时,加入的KIO3为_________mol 。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子 Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过分析,认为无需 检验就可判断其中必有的两种物质是和(填化学式)。
检验就可判断其中必有的两种物质是和(填化学式)。
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记C,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时也产生红褐色沉淀,向该沉淀中滴人稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解。则X为。
A.SO32-B.SO42-C.CH3COO- D.SiO32-
(3)B的水溶液显性,原因为。(用离子方程式表示)
(4)将0.02 molA与0.0 1molC同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的物质的量为(保留一位小数)
(5)将Cu投人到装有D溶液的试管中,Cu不溶解;再 滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的
滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的 (填相应的离子符号)。有关反应的离子方程式为:。
(填相应的离子符号)。有关反应的离子方程式为:。
(6)利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论。