碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素。在实验室中,从海藻里提取碘的流程和实验装置如下: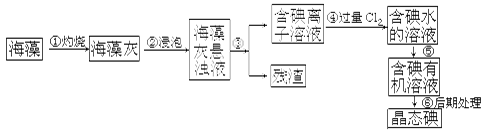
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③_______________,
步骤 _______________。
_______________。
(2)写出步骤④对应反应的离子方程式:______________________________。
(3)提取碘的过程中,可供选择的有机试剂是_______________。
| A.酒精 | B.醋酸 | C.四氯化碳 | D.苯 |
(4)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至 ,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是_________________________________________________________。
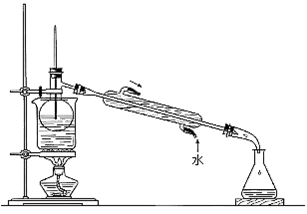
,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是_________________________________________________________。 (5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处: 。
(5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处: 。
有一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是_________;X与氢元素形成的化合物的电子式是_______________。
(2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________;D与E能形成一种分子,该分子的结构式为__________________;D所在族元素的氢化物中,沸点最低的是(填名称)_________;X与E形成的离子化合物 XE2中(填“有”“无”)共价键。
(3)短周期元素W与Y同周期其单质是半导体材料;元素Z的单质分子Z2中由3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是_________。
(4)用化学式回答:①D与Y的氢化物稳定性____>______ ;
;
②最高价氧化物对应水化物酸性____> ____。
下图为周期表中的一部分。已知A、B、C、D均为短周期元素,A与D原子序数之和为C原子序数的1 .5倍。
(1)B元素符号是: _______、D在元素周期表中第_______族。
(2)四种元素中原子半径最大的是(填元素符号)_______,B、C、D三种离子中半径最大的是(填离子符号)_______。
(3)B比C的氢化物的沸点高是因为_______;A、D两元素的气态氢化物相互反应的生成物的电子式:,其中存在_______键、_______(填“极性”或“非极性”)共价键。
(4)写一个离子方程式证明C和D的非金属性相对强弱:。
在水溶液中有质子数相同,电子数也相同的A、B、C三种离子。A、B都能与阴离子D反应,D的电子总数与A相等,但质子总数比A少2个。A与D反应生成分子中电子总数与A相等,但质子总数比A少1的气体E。B与D反应时生成的分子中电子总数、质子总数与E都相等的液体F。则A~F的化学式或符号分别为:
A______;B________;C________;D________;E________;F________。
试回答下列各问题:
(1)如图Ⅰ所示是1 mol NO2和CO反应生成 CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:。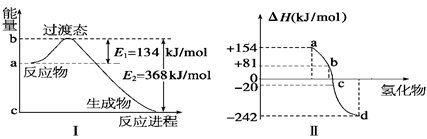
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g)="==" 2HCl(g) ΔH="-185" kJ/mol;
键能ΔH298(H—H)="436" kJ/mol,ΔH298(Cl—Cl)="247" kJ/mol,则ΔH298(H—Cl)=。
②图Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲生成氢化物时的焓变数据,根据这组焓变数据可确定a、b、c、d分别代表的元素,试写出硒化氢发生分解反应的热化学方程式:。
(3)已知: ①Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g)ΔH="-a" kJ/mol
2Fe(s)+3CO2(g)ΔH="-a" kJ/mol
②3Fe2O3(s)+CO(g)  2Fe3O4(s)+CO2(g)ΔH="-b" kJ/mol
2Fe3O4(s)+CO2(g)ΔH="-b" kJ/mol
③Fe3O4(s)+CO(g)  3FeO(s)+CO2(g)ΔH="+ckJ/mol"
3FeO(s)+CO2(g)ΔH="+ckJ/mol"
则FeO(s) +CO(g)  Fe(s)+CO2(g)ΔH=-。
Fe(s)+CO2(g)ΔH=-。
已知:
① N2 (g) + 2O2 (g) = 2NO2 (g)△H1 =" +" 67.7kJ/mol
②N2H4 (g) +O2 (g) = N2(g) +2H2O (g)△H2 = -534kJ/mol
③1/2H2 (g) + 1/2F2 (g) = HF (g)△H3 = -269kJ/mol
④H2 (g) + 1/2O2 (g) = H2O (g)△H4 = -242kJ/mol
⑤H2O(l)====H2O(g) △H5=+44kJ·mol-1
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出液态肼和足量H2O2反应的热化学方程式_______________________________。
(2)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(3)16 g气态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(4根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式____________________________________。
(5)有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,肼和氟反应的热化学方程式:。