可用于分离或提纯物质的方法有:①过滤 ②蒸馏 ③加热分液(填序号)
(1)除去石灰水中悬浮的CaCO3颗粒
(2)除去NaCl晶体中混有的碘单质
(3)分离石油中各不同沸点范围的成分
(4)分离水和苯的混合物
(5)分离CCl4(沸点76.75℃)和甲苯(沸点110.6℃)____________。
X、Y、Z、R、W为五种原子序数依次增大的短周期元素。
已知:①X元素的原子半径是所有原子中最小的;
②Y元素的原子最外层电子数是最内层电子数的2倍。
③Y与R可以形成YR与YR2两种化合物,其中一种是造成温室效应的物质之一。
④W与R能形成原子个数之比为2:1和1:1的离子化合物甲和乙。
根据要求回答问题:
(1)R在周期表中的位置是_______________;甲的电子式是___________。
(2)元素Y、R的最简单氢化物的稳定性由大到小顺序为(填化学式)。
(3)X2R与乙反应的化学方程式是__________________。
(4)元素Y、R、W形成的化合物的水溶液常用作清洗厨房的油污,其原理是(用离子方程式表示)。欲使0.1mol·L-1该溶液中浓度最大的阳离子与浓度最大的阴离子浓度之比=2,可以加入的物质是(填一种)。
化学链燃烧是将燃料与载氧体再被空气氧化再生,以实现较低温度下燃烧的过程。该过程具有无火焰、低污染、高效率的特点。
(1)用煤作燃料时,需要先用H2O或CO2将煤转化为燃料气。950℃时,焦炭被H2O氧化后产物的体积分数如图所示、其中H2含量较多的原因是、(用化学方程式表示)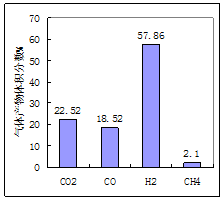
(2)燃料反应的气体产物主要是H2O和CO2通过(填操作名称)分离出水,并回收CO2。
(3)CaSO4是一种载体,请写出CaSO4与H2反应的化学方程式;CO还原载体CaSO4的主要反应是①,副反应是②
①CaSO4( s)+4CO(g)=CaS(s)+4CO2(g) △H=-175.6 kJ.mol-1
②CaSO4(s)+CO(g)=CaO(s)+CO2(g)+SO2(g) △H=+218.4 kJ.mol-
右图是CO与CaSO4在900℃反应后,固体的物质的量分数与n(CaSO4)/n(CO)的关系图。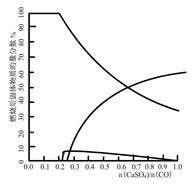
当n(CaSO4)/n(CO)>0.25时,产生对环境影响的气体是,你的理由。
硼及其化合物在工业生产中应用广泛。用硼镁矿(主要成分Mg2B2O5.H2O)采用碳铵法生产硼酸主要流程如下:

(1)硼镁矿焙烧时需要粉碎,其目的是。硼镁矿焙烧过程中只生成两种物质,写出化学方程式。
(2)硼酸溶解度如下所示,从NH4H2BO3溶液获得硼酸晶体蒸发浓缩、冷去结晶、过滤、洗涤、干燥获得硼酸晶体。洗涤过程中需要用(填“冷水”或“热水”),你的理由是。
(3)测得硼酸晶体纯度的试验方法是,取0.5000g样品与锥形瓶中,加甘油和刚冷却的废水,微热使样品溶解,迅速冷却至室温,加酚酞指示剂,用NaOH标准溶液滴定至15.80ml时,溶液恰好显粉红色且半分钟不褪色。
已知:每1.00mlNaOH滴定液相当于30.92mg的H3BO3
①迅速冷却锥形瓶中溶液的方法是;
②滴定实验中加入甘油的目的;
③测该样品中H3BO3的质量分数为;
X、Y、Z、W四种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
空气含量最多的元素 |
| Y |
3p能级只有一个电子 |
| Z |
单质用于制造集成电路和太阳能板的主要原料 |
| W |
常见化合价有+2、+3,其中一种氧化物为红褐色 |
(1)W位于周期表的第周期,第族。
(2)用“>”或“<”填空。
| 离子半径 |
电负性 |
第一电离能 |
单质熔点 |
| X Y Z |
ZW |
XZ |
XW |
(3)X2、碳和Z的氧化物在1300℃时可合成Z3X4。写出该反应化学方程式。Z3X4是一种耐高温的结构陶瓷材料,是化合物(填“共价”或“离子”)。
(4)查阅资料知道:
4Y(s)+3O2(g)=2Y2O3(s) △H=-3351.4 kJ.mol-1
3W(s)+2O2(g)=W3O4(s) △H=-1120 kJ.mol-1
则Y与W3O4反应的热化学方程式是:。
某无色溶液X,由Na+、Ag+、Ba2+、Al3+、[Al(OH)4]--、MnO4—、CO32--、SO42—中的若干种离子组合,取溶液进行如下连续试验:(填化学用语)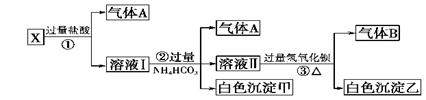
(1)气体A的成分是:_________________,气体B的成分是_____________
(2)X溶液中一定存在的离子是:____________________________
(3)写出步骤①发生反应的所有离子反应方程式:_________________________
(4)写出步骤②形成白色沉淀甲的离子方程式:______________________
(5)写出白色沉淀乙的可能组成:____________________________