用中和滴定法测定某烧碱样品的纯度。有以下步骤:
(1)配制待测液:用5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液。除烧杯和玻棒外,还需要的玻璃仪器有___________________________.
(2)滴定:①盛装0.1000 mol/L的盐酸标准液应该使用_______式滴定管。
②滴定时双眼应_________________________________________________.
(3)有关数据记录如下:
| 测定序号 |
待测溶液的体积(mL) |
所耗盐酸标准液的体积(mL) |
|
| 滴定前读数 |
滴定后读数 |
||
| 1 |
20.00 |
0.50 |
20.78 |
| 2 |
20.00 |
1.20 |
21.32 |
计算纯度:烧碱样品的纯度是__________________;
(取两次实验所耗盐酸的平均值进行计算)
(4)误差讨论:(选填“偏高”、“偏低”或“无影响” )
① 用蒸馏水冲洗锥形瓶,会使测定结果____________;
② 在滴定过程中不慎将数滴酸液滴在锥形瓶外,会使测定结果____________;
③ 读数时,滴定前仰视,滴定后俯视,会使测定结果____________;
④ 装标准液之前,没有用标准液润洗滴定管,会使测定结果____________。
(13分)某研究性学习小组用下图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。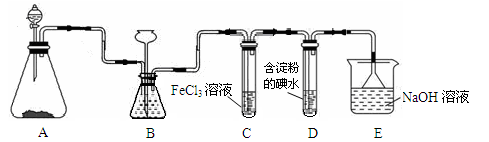
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在中,再加水稀释。
(2)下列实验方案适用于在装置A中制取所需SO2的是。
a.Na2SO3固体与浓硝酸 b.Na2SO3固体与浓硫酸
c.CaSO3固体与稀硫酸 d.碳与热的浓硫酸
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)往FeCl3溶液中通入足量SO2,反应的离子方程式为。
(5)能表明SO2的还原性强于I-的反应现象为__________________。
(6)装置E的作用为________________。
(7)在上述装置中通入过量的SO2,为了验证C中SO2与Fe3+发生了氧化还原反应,取C中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是,理由是。
从有机反应R—H+Cl2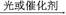 R—Cl+HCl制取副产品盐酸的设想已成为现实。请根据所给模拟装置图回答下列问题:
R—Cl+HCl制取副产品盐酸的设想已成为现实。请根据所给模拟装置图回答下列问题: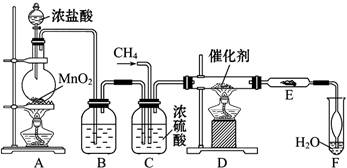
(1)写出实验室制Cl2的离子方程式____________________________________
(2)装置B中盛放的溶液是___________________,作用是____________________。
(3)装置C有三种功能:①_______________;②_______________;③观察气泡的产生情况,便于控制两种气体的配比。
(4)玻璃管E中放在石棉碎块上的碘化钾的作用是:______________。导管末端“肚形”装置的作用是_____________________。
(5)从F中分离出盐酸的最佳方法是_________。该套实验装置还存在的缺陷是。
(共8分)溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。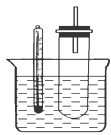
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL溴乙烷,振荡。
实验操作Ⅱ:将试管如图固定后,水浴加热。
(1)(每空1分)用水浴加热而不直接用酒精灯加热的原因是;试管口安装一长导管的作用是。
(2)(每空1分)鉴定生成物中乙醇的结构,可用的波谱是,。
(3)(每空2分)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是,检验的方法是(需说明所用的试剂、简单的实验操作及预测产生的实验现象)。
(共14分)下图为苯和溴的取代反应的改进实验装置图。其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入铁屑粉少量。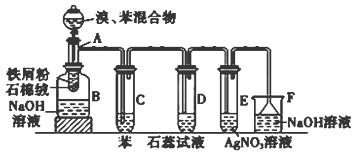
填写下列空白:(注:溴苯与NaOH溶液不可以发生水解反应)
(1)(每空2分)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式)_____________。
(2)(每空2分)试管C中苯的作用是______;反应开始后,观察D和E试管,看到的现象为D中_________;E中;
(3)(每空2分)反应2 min至3 min后,在B中的NaOH溶液可观察到的现象是。
(4)(每空2分)在上述整套装置中,具有防倒吸的仪器有_______(填字母)
(5)(每空2分)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点是_______________。
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
| 实验操作 |
实验现象 |
| ⅰ.打开A中分液漏斗活塞,滴加浓硫酸 |
A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ⅱ.取C中沉淀加入盐酸 |
C中白色沉淀不溶解 |
| ⅲ.打开B中分流漏斗活塞,逐滴滴加H2O2 |
开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)A中发生反应的化学方程式是_______________________
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是_____________。
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是____________
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)ⅲ中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br―
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是___________________________________
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是________。