(14分)(1)向1 L AlCl3和FeCl3混合溶液中加入含a mol NaOH的溶液时,产生的沉淀量可达最大值;继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到b mol时,沉淀不再减少,则原溶液中Fe3+的物质的量浓度为 ,AlCl3的物质的量 。
(2)已知:2Fe3++2I- = 2Fe2++ I2; 2Fe2++Br2 = 2Fe3++2Br-
①向含有1mol FeI2和1.5mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是 。
②如果向①的溶液中通入3mol Cl2,则被氧化的离子对应的氧化产物分别是 。
(3)①若m g铁屑与含有 n gHNO3的硝酸溶液恰好完全反应,若 m : n =" 1" : 2.7, 该反应的化学方程式为 __________________________________________________(假设还原产物只有一种,且只生成一种盐)
②若含 n g HNO3的稀硝酸溶液恰好使5.6g铁粉完全溶解,若有 n/4 gHNO3被还原成NO(无其它还原产物)则 n 的范围为_________________________
③某条件下锌和硝酸反应时的物质的量之比为2:5,此时硝酸的还原产物是____________
苄佐卡因是一种医用麻醉药品,学名对氨基苯甲酸乙酯,它以对硝基甲苯为主要起始原料经下列反应制得:
请回答下列问题:
(1)写出A、B的结构简式:A____________,B___________
(2)化合物C中含有的官能团名称是:、 。
(3)写出由A和B化合反应生成C的化学反应方程式
该反应属于 (填反应类型)
(填反应类型)
(4)苄佐卡因(D)的水解反应如下: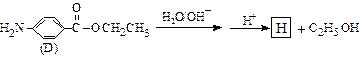
化合物H经聚合反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域。
请写出该聚合反应的化学方程式______________________ ____________________。
____________________。
碳和碳的化合物在生产生活实际中应用广泛。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知 ① 2 CH4 (g) + 3O2 (g) = 2 CO (g) + 4 H2O(l) △H1 = -1214.6 KJ/mol
② 2 CO (g) + O2(g) = 2 CO2 (g)△H2 = -566 kJ/mol
则反应CH4(g) + 2 O2 (g) = CO2 (g) + 2 H2O (l) 的△H = 。
(2)若用石墨做电极电解饱和食盐水,则电解反应的离子方程式为: ;
(3)将不同量的CO (g) 和H2O (g) 分别通入到体积为1L的恒容密闭容器中,进行反应 CO (g) + H2O (g) CO2 (g) + H2 (g),得到如下三组数据:
CO (g) + H2O (g) CO2 (g) + H2 (g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所 需时间/min |
||
| H2O |
CO |
CO2 |
CO |
|||
| 1 |
650 |
2 |
4 |
1.6 |
2.4 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
1.6 |
3 |
| 3 |
900 |
2 |
4 |
0.8 |
3.2 |
2 |
① 实验1中以υ(H2) 表示的反应速率为 。
② 实验2中的平衡常数是 (计算结果保留两位小数)。
③ 该反应的正反应为 (填“吸”或“放”)热反应。
在右下图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重6.4g。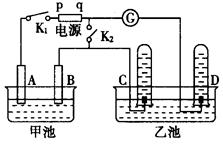
请回答下列问题:
(1)B电极发生反应的电极反应式。
C电极发生反应的电极反应式.
(2)甲池电解时反应的离子方程式。
(3)甲池电解后溶液的c(H+)为,要使电解后溶液恢复到电解前的状态,则需加入,其质量为g。(假设电解前后溶液的体积不变)
(4)请你设计实验确定甲池原溶液中可能含有的酸根离子,要求:提出两种可能的假设,分别写出论证这两种假设的操作步骤、实验现象和实验结论
①假设一:; ②假设二:。
②假设二:。
(5)若再将K1断开,闭合K2,灵敏电流计中指针是否会发生偏转?理由是什么?
如右图所示,A、B、C三个装置中的三个烧杯分别盛有足量的CuCl2溶液。
A(左Zn右Cu) B(左C右Pt) C(左Zn右Cu)
(1)、A、B、C三个装置中属于原电池的是_____ (填标号,下同),属于电解池的是____________。
(2)、A池中Zn是_______极,发生_______反应(填“氧化”或“还原”,下同),电极反应式为_________; Cu是_____极, 发生_____反应, 电极反应式为,A中总反应的化学方程式为。
(3)、B池中C是_____极,发生_____反应,电极反应为;Pt是_____极,发生______反应,电极反应为。B池中总反应的化学方程式为 ________________。
(4) C池中Zn是_____极,发生______反应,电极反应为_______________;Cu是极, 发生反应, 电极反应为反应过程中,溶液浓度________(填“变大”“变小”或“不变”)。
30、从H+、Cu2+、Na+、Ag+ 、NO3-、SO42-、Cl- 七种离子中恰当地组成电解质,按下列要求进行电解:
(1)以碳棒为电极,使电解质质量减少,水质量不变,进行电解,则可采用的电解质是
。
(2)以碳棒为电极,使电解质质量不变,水质量减少,进行电解,则可采用的电解质是
。
(3)以碳棒为阳极,铁棒为阴极,使电解质和水质量都减少,电解后生成碱和氢气,则电解质为。
(4)以碳棒为阳极,铁棒为阴极,使电解质和水质量都减少,电解后生成酸和氧气,,则电解质为。