Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备Na2CO3。下面是他的制备实验过程:用50 mL NaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量,生成NaHCO3,他设计了如下实验步骤:
(I)用25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
(Ⅱ)小心煮沸溶液1~2分钟;
(Ⅲ)在得到的溶液中加入另一半(25 mL)NaOH溶液,使溶液充分混合。
(1)在(I)中,刚通入CO2时发生的反应化学方程为 而后又发生反应的离子方程式为
在(Ⅱ)中煮沸溶液的目的是
在(Ⅲ)中混合另一半NaOH溶液后发生的反应的离子方程式是 。
(2)按该同学的设计,第(I)步实验装置如下: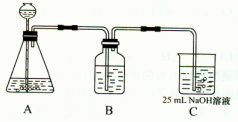
①装置A使用的试剂是 (固体)和 ;
②装置B使用的试剂最好是 (选择:水、饱和NaOH溶液、饱和Na2CO3溶液、饱和NaHCO3溶液),作用是 ,如果不用B装置,最终得到的Na2CO3溶液中可能存在的杂质有 。
已知NaBiO3是黄色、微溶于水的固体;Bi3+为无色。将NaBiO3固体加入到MnSO4和H2SO4的混合溶液中,加热,得紫色的混合溶液。试写出该反应的离子方程式。
填空题:
盐酸、硫酸和硝酸是三种重要的酸。
(1)工业上生产盐酸与硝酸时,都要用到的气态反应物是_______;
(2)工业上生产硫酸与硝酸时,用到的相同的重要设备是_______;
(3)工业生产中欲制得高浓度的硫酸与硝酸,可使用的相同物质是_______;
(4)浓盐酸与浓硝酸暴露在空气中,相同的现象是_______;
(5)浓硫酸与浓硝酸都可用铁、铝容器贮存的相同原理是_______;
(6)实验室制备H2、CO2、H2S、SO2时,用盐酸和浓硫酸可制备的相同气体是_______。
某溶液A,可能含有等物质的量浓度的SiO32-、CO32-、SO32-、S2-、AlO2-、Cl-、PO43-中的几种,现进行以下实验:
(1)以10mLA溶液,往其中通入足量的CO2,得到白色沉淀B,B可完全溶于稀硫酸。
(2)另取10mLA溶液,往其中加入稀硫酸,生成气体C,将C通入Pb(NO3)2溶液中,有黑色沉淀D生成。
问题:
(1)溶液A中肯定存在:_____________________________________.
(2)溶液A中肯定不存在:______________________________,其理由是:___________________.
有一瓶无色气体,可能含有HCl、H2S、CO2、HBr、SO2中的一种或几种,将其通入氯水中得无色透明溶液,把溶液分成两份,向一份中加入盐酸酸化的BaCl2溶液,出现白色沉淀;另一份中加入硝酸酸化的AgNO3溶液,也有白色沉淀,以下结论正确的是……( )
①原气体中肯定有SO2,②原气体中可能有SO2,③原气体中肯定没有H2S、HBr,④不能肯定原气体中是否含有HCl,⑤原气体中肯定无CO2,⑥原气体中肯定有HCl.
| A.①③④ | B.②④ | C.①③⑥ | D.①③⑤⑥ |
某溶液中含有较多的Na2SO4和少量的 Fe2(SO4)3。若用该溶液制取芒硝(Na2SO4·10H2O),可供选择的操作有:
①加适量H2SO4溶液;②加金属钠;③结晶;④加过量NaOH;⑤加强热脱结晶水;⑥过滤。正确的操作步骤是
| A.②⑥③ | B.④⑥①③ | C.④⑥③⑤ | D.②⑥①③⑤ |