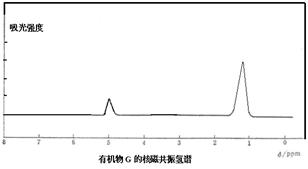
某有机物A的分子式为C6H10Br2,不能使溴水褪色,G的分子式为C4H8,能使溴水褪色,A、G的核磁共振氢谱如下。G为石油化工基本原料,K为高分子化合物,1mol J与足量金属钠反应生成22.4L(标准状况)氢气,C、D互为同分异构体。各有机物之间的转化关系如下:
已知: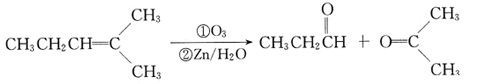
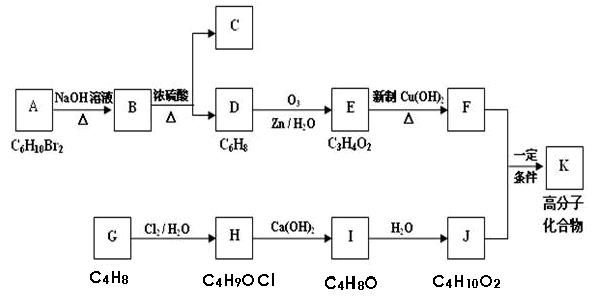
回答下列问题:
(1)C的结构简式为 ,
(2)写出B→D的化学方程式 。
(3)A在一定条件下也能直接反应生成D,写出相应的化学方程式(需注明反应条件)
(4)写出F和J反应生成K的化学方程式
(5)有机物R与B互为同分异构体,满足下列条件的R共有 种,写出任意的两种
① 与NaOH溶液反应 ②不能与NaHCO3溶液反应 ③碳链无支链
(10分)下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语回答下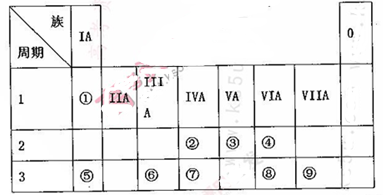
列问题:
(1)画出表中形成化合物种类最多元素的原子结构示意图____;写出它与原予半径最小的原子形成10电子且为正四面体结构的化合物的电子式____,用电子式表示⑤和⑧形成化合物的过程________。
(2).④⑤⑧形成的简单离子半径由大到小的顺序为____(填离子符号);③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为_______(填化学式)。
(3).⑤和⑨形成化合物的化学键为__________。
(4).这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是_______(填化学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式___________________________。
某有机物A由C、H、O三种元素组成,90克A完全燃烧可生成132克CO2和54克H2O。试求:
①该有机物的最简式________。
②若符合该最简式的A物质可能不止一种,则它们之间的关系________(填序号)
A.一定互为同系物B.一定互为同分异构体
C.等质量的它们完全燃烧耗氧量相同 D.等物质的量的它们完全燃烧耗氧量相同
③若A的相对分子质量为180,每个碳原子上最多只有一个官能团,能发生银镜反应,也能发生酯化反应,且所有碳原子在同一链上,则A的结构简式为________。
巨豆三烯酮(F)是一种重要的香料,其合成路线如下:
(1)化合物F的分子式为________,1 mol该物质完全燃烧需消耗________mol O2。
(2)在上述转化过程中,反应②的目的是________,写出反应②的化学方程式为________。(3)下列说法正确的是________(双选,填字母)。
A.化合物A ~ F均属于芳香烃衍生物
B.反应①属于还原反应
C.1 mol 化合物D可以跟4 mol H2发生反应
D.化合物F含有的官能团名称为碳碳双键、羰基
(4)符合下列条件的D的同分异构体有两种,其中一种同分异构体的结构简式为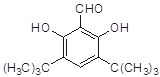 ,请写出另外一种同分异构体的结构简式________。
,请写出另外一种同分异构体的结构简式________。
A.属于芳香族化合物;
B.核磁共振氢谱显示,分子中有4种化学环境不同的氢原子;
C.1mol该物质最多可消耗2molNaOH
D.能发生银镜反应。
化学式为C5H12O的有机物,可与金属钠反应产生氢气,试根据下列性质按要求填空。
(1)若该有机物可去氢被氧化成羰基化合物,而不能发生脱水消去反应,则该有机物可能氧化生成的羰基化合物的结构简式为。名称
(2)若该有机物不能去氢被氧化成羰基化合物,而能发生脱水消去反应,则该有机物的结构简式可能为。名称
完成下列化学方程式(8分)
(1) 与足量金属钠发生反应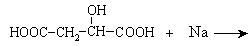
(2) 与NaOH的醇溶液共热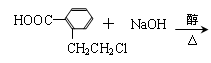
(3) 葡萄糖和新制Cu(OH)2及NaOH共热
(4)与足量H2反应
OHC-CH=CH-COOH+H2