在碱性溶液中,下列各项中的离子可以大量共存的是
| A.Fe3+、Cu2+、Cl—、NO3— | B.K+、NO3—、Ag+、Cl— |
| C.Na+、SO42—、K+、Cl— | D.Ca2+、MnO4—、Na+、CO32— |
某探究小组利用丙酮的溴代反应:( )
)
来研究反应物浓度与反应速率的关系。反应速率 通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据( )
通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据( )

 分析实验数据所得出的结论不正确的是
分析实验数据所得出的结论不正确的是
A.增大 增大 增大 |
B.实验②和③的 相等 相等 |
C.增大  增大 增大 |
D.增大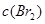 , , 增大 增大 |
对于可逆反应:2A(g)+B(g)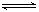 2C(g);△H<0,下列图象正确的是( )
2C(g);△H<0,下列图象正确的是( )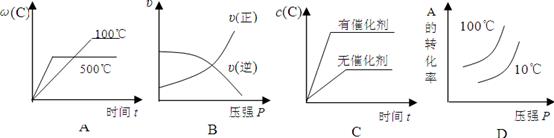
下列叙述不正确的是( )
| A.铁表面镀锌,铁作阳极 |
| B.船底镶嵌锌块,锌作负极,以防船体被腐蚀 |
C.钢铁吸氧腐蚀的正极反应: |
D.工业上电解饱和和食盐水的阴极反应:2H+ +2e –= 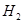 ↑ ↑ |
在密闭容中发生下列反应aA(气) cC(气)+dD(气),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(气)+dD(气),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
| A.平衡向正反应方向移动 | B.A的转化率变小 |
| C.D的体积分数变大 | D.a >c+d |
已知蓄电池在放电时起原电池的作用,充电时起电解池的作用。铅蓄电池在放电和充电 时发生的化学反应可用下式表示:
时发生的化学反应可用下式表示: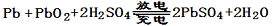
据此判断下列叙述中正确的是 ( )
A.放电时正极电极反应式PbO2 + SO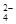 + 2e – + 4 H+= PbSO4 + 2H2O + 2e – + 4 H+= PbSO4 + 2H2O |
| B.充电时蓄电池负极应与电源正极相连接 |
| C.充电时,若要使1mol PbSO4转变为PbO2,则需要通过4mol电子 |
| D.电池放电时,溶液酸性增强 |