50 mL密度为1.84 g·cm-3,质量分数为98%的浓H2SO4,其H2SO4的物质的量浓度为 。若将50 mL该浓H2SO4稀释成密度为1.47 g·cm-3的溶液100mL,需水 mL。(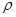 水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
水=1g·cm-1)稀释后溶液的质量分数为 ,物质的量浓度为 。
[化学——有机化学基础]
Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。结构简式如图。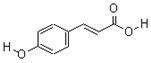
(1)该有机物具有的官能团名称是(写出其中的两种)。
(2)该有机物能发生的反应类型是(填写代号)。
A.氧化反应 B.消去反应 C.加聚反应 D.水解反应
Ⅱ.芳香族化合物C10H10O2有如下的转化关系: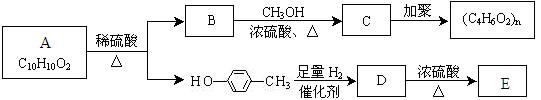
已知E能使Br2/CCl4溶液褪色。请回答下列问题:
(3)请分别写出A、E的结构简式A E。
(4)若有机物F与C互为同分异构体,则与有机物B为同系物的F的同分异构体有种
(5)请写出B→C反应的化学方程式。
[化学——物质结构与性质]
已知A、B、C、D、E五种元素的原子序数依次增大,其中A、E原子的最外层电子数均等于其周期序数,E原子的电子层数是A的3倍;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子。请回答下列问题:
(1)E元素基态原子的电子排布式为。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为(填元素符号)。
(3)D元素与氟元素相比,电负性:DF(填“>”、“=”或“<”)。
(4)BD2在高温高压下所形成的晶体其晶胞如图所示。该晶体的类型属于(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子轨道的杂化类型为。l mol B2A2分子中含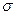 键的数目是。
键的数目是。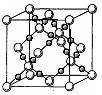
(5)光谱证实单质E与强碱溶液反应有[E(OH)4]—生成,则[E(OH)4]—中存在。
a.共价键 b.配位键 c.σ键 d.π键
物质A、B、C有如下转化关系: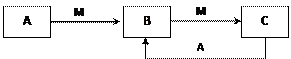
请回答下列问题:
(1)若A、B、C均为含铝元素的化合物,M可以是 。
(2)若M是第IVA族某元素的最高价氧化物,且M为气体,组成A的阴阳离子均含有10个电子,请写出C的名称 
(3)若A是一种黄绿色气体,M是一种常见金属。写出C→B的离子方程式
。
(4)若A、B、C都是含硫化合物,已知:
A转化为B的热化学方程式:2H2S(g)+ O2(g) =2S (s)+2H2O(l) △H= -a kJ·mol-1;
A转化为C的热化学方程式:2H2S(g)+ 3O2(g) =2SO2(g)+2H2O(l) △H= -b kJ·mol-1;
请写出A与C反应转化为B的热化学方程式。
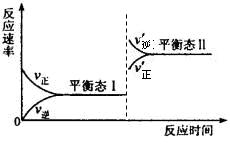
(5)若C+A→B的转化关系为4NH3+6NO 6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系如图。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)
6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系如图。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为: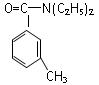
已知:RCOOH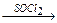 RCOCl(酰氯);RCOCl + NH3→RCONH2 + HCl,
RCOCl(酰氯);RCOCl + NH3→RCONH2 + HCl,
避蚊胺在一定条件下,可通过下面的合成路线I来合成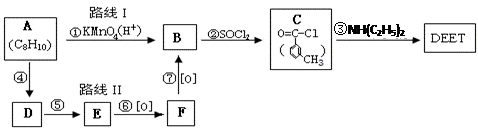
根据以上信息回答下列问题:
(1)由避蚊胺的结构简式推测,下列叙述正确的是。
| A.它能使酸性高锰酸钾溶液褪色 | B.它能发生酯化反应 |
| C.它与甲苯互为同系物 | D.一定条件下,它可与H2发生加成反应 |
(2)在反应①~⑦中,属于取代反应的有(填序号)。
(3)写出下列化学反应方程式:
C→DEET;
E→F。
(4)经测定E的同分异构体能与FeCl3溶液发生显色的反应,且结构中不含乙基,试写出符合其条件的任意2个可能的结构简式。
(5)经核磁共振氢谱图显示A的某种同分异构体J只有两个吸收峰(及两种环境的氢原子),试写出J的化学名称;J物质被酸性高锰酸钾氧化后得到的产物在一定条件下可与乙二醇反应,制成涤纶(聚酯纤维),试写出生产涤纶的化学方程式。
恒温、恒压下,在一个可变容积的容器中发生如下发应:
A(气)+B(气)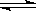 C(气)
C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x=mol,y=mol。
平衡时,B的物质的量(选填一个编号)
(甲)大于2 mol(乙)等于2 mol
(丙)小于2 mol(丁)可能大于、等于或小于2mol
作出此判断的理由是。
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是。若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA和1molB到达平衡后生成b molC。将b与(1)小题中的a进行比较(选填一个编号)。
(甲)a<b(乙)a>b(丙)a=b(丁)不能比较a和b的大小
作出此判断的理由是。