避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为: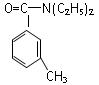
已知:RCOOH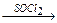 RCOCl(酰氯);RCOCl + NH3→RCONH2 + HCl,
RCOCl(酰氯);RCOCl + NH3→RCONH2 + HCl,
避蚊胺在一定条件下,可通过下面的合成路线I来合成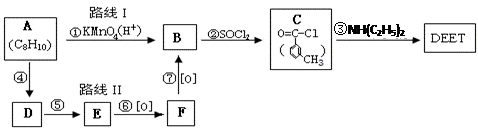
根据以上信息回答下列问题:
(1)由避蚊胺的结构简式推测,下列叙述正确的是 。
| A.它能使酸性高锰酸钾溶液褪色 | B.它能发生酯化反应 |
| C.它与甲苯互为同系物 | D.一定条件下,它可与H2发生加成反应 |
(2)在反应①~⑦中,属于取代反应的有 (填序号)。
(3)写出下列化学反应方程式:
C→DEET ;
E→F 。
(4)经测定E的同分异构体能与FeCl3溶液发生显色的反应,且结构中不含乙基,试写出符合其条件的任意2个可能的结构简式 。
(5)经核磁共振氢谱图显示A的某种同分异构体J只有两个吸收峰(及两种环境的氢原子),试写出J的化学名称 ;J物质被酸性高锰酸钾氧化后得到的产物在一定条件下可与乙二醇反应,制成涤纶(聚酯纤维),试写出生产涤纶的化学方程式 。
已知下列热化学方程式:
①H2(g)+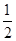 O2(g)=H2O(l)ΔH=-285.8 kJ/mol
O2(g)=H2O(l)ΔH=-285.8 kJ/mol
②H2(g)+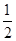 O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol
③C(s)+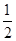 O2(g)=CO(g)ΔH=-110.5 kJ/mol
O2(g)=CO(g)ΔH=-110.5 kJ/mol
④C(s)+O2(g)=CO2(g)ΔH=-393.5 kJ/mol
回答下列问题:
(1)上述反应中属于放热反应的是。
(2)H2的燃烧热为,C的燃烧热为。
(3)燃烧10 g H2生成液态水,放出的热量为。
(4)CO的燃烧热为,其热化学方程式为。
已知某反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,回答问题。
该反应是(填“吸热”或“放热”)反应,该反应的ΔH=kJ/mol(用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量(填“一定高”“一定低”或“高低不一定”)。
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH=+260 kJ/mol
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
则CH4与O2反应生成CO和H2的热化学方程式为。
已知反应①Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=akJ·mol-1,平衡常数为K;
FeO(s)+CO(g) ΔH=akJ·mol-1,平衡常数为K;
反应②CO(g)+1/2O2(g) CO2(g) ΔH=bkJ·mol-1;
CO2(g) ΔH=bkJ·mol-1;
反应③Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=ckJ·mol-1。测得在不同温度下,K值如下:
2Fe(s)+3CO2(g) ΔH=ckJ·mol-1。测得在不同温度下,K值如下:
| 温度/℃ |
500 |
700 |
900 |
| K |
1.00 |
1.47 |
2.40 |
(1)若500 ℃时进行反应①,CO2的起始浓度为2 mol·L-1,CO的平衡浓度为 。
(2)反应①为 (选填“吸热”或“放热”)反应。
(3)700 ℃时反应①达到平衡状态,要使该平衡向右移动,其他条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积 B.通入CO2
C.温度升高到900 ℃ D.使用合适的催化剂
E.增加Fe的量
(4)下列图像符合反应①的是 (填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2)。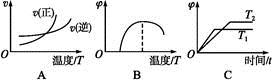
(5)由反应①和②可求得,反应2Fe(s)+O2(g) 2FeO(s)的ΔH= 。
2FeO(s)的ΔH= 。
(6)请运用盖斯定律写出Fe(固体)被O2(气体)氧化得到Fe2O3(固体)的热化学方程式: 。
孔雀石主要含Cu2(OH)2CO3,还含少量铁的化合物和硅的化合物。以孔雀石为原料可制备CuCl2·3H2O及纯碱,流程如图所示。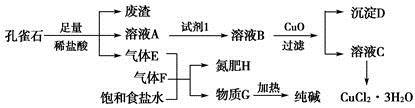
已知:溶液A只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH如表所示。回答下列问题:
| 金属离子 |
Fe3+ |
Fe2+ |
Cu2+ |
|
| pH |
氢氧化物 开始沉淀 |
1.9 |
7.0 |
4.7 |
| 氢氧化物 完全沉淀 |
3.2 |
9.0 |
6.7 |
(1)图中“试剂1”为________。
(2)加入CuO的作用是调节溶液pH,则pH的范围为________。
(3)气体E、F与饱和食盐水作用生成H和G时,E和F应按一定先后顺序通入饱和食盐水中。其中,应先通入的气体是________(填代号及对应物质的化学式)。
(4)由溶液C获得CuCl2·3H2O,需要经过__________、________、过滤等操作。
(5)已知:常温下Cu(OH)2的Ksp=2×10-20。计算Cu2++2H2O Cu(OH)2+2H+的平衡常数为________。
Cu(OH)2+2H+的平衡常数为________。