某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:
3A(g)+2B(g) 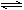 4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K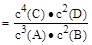 |
| B.此时,B的平衡转化率是40% |
| C.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
| D.增加B,平衡向右移动,B的平衡转化率增大 |
某温度下的密闭容器中发生如下反应:2M(g)+N(g) 2E(g),若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2molM和1molN的混合气体,则达平衡时M的转化率为()
2E(g),若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2molM和1molN的混合气体,则达平衡时M的转化率为()
| A.20% | B.40% | C.60% | D.80%  |
在容积不变的密闭容器中,一定条件下进行如下反应:
NO(g)+CO(g)===0.5N2(g)+CO2(g);ΔH=-373.2kJ·mol-1。下图曲线a表示该反应过程中,NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是()
|
| A.加催化剂 |
| B.向密闭容器中加入氩气 |
| C.降低温度 |
| D.增大反应物中NO的浓度 |
pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000mL,其pH值与溶液体积的关系如图,下列说法正确的是()
 |
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液强
C.若1< a < 4,则A、B都是弱酸
D.若a = 4,则A是弱酸,B是强酸。
酸碱指示剂一般是有机弱酸(用Hln表示)或弱碱,其分子形式与电离出的ln—形式颜色不同,在pH值不同的溶液中至所以能表现出不同的颜色,是因为其电离平衡发生移动的结果。甲基橙是一种常用的酸碱指示剂,溶于水后发生如下电离:Hln H++ln—,已知在pH<3.1的溶液中呈红色,在pH>4.4的溶液中呈黄色,下列判断中不正确的是()
H++ln—,已知在pH<3.1的溶液中呈红色,在pH>4.4的溶液中呈黄色,下列判断中不正确的是()
| A.Hln呈红色 |
B.ln—呈黄色 |
| C.遇pH值介于3.1~4.4的溶液可能呈橙色 |
| D.Hln呈黄色 |
常温下,向一定浓度的氨水中逐滴加入盐酸,关于溶液中各离子浓度大小关系叙述最准确的是()
| A.c(Cl—)> c(NH4+) > c(H+) > c(OH—) |
| B.c c(NH4+) = c(Cl—) > c(H+) = c(OH—) |
| C.c(NH4+) > c(Cl—) > c(OH—) > c(H+) |
| D.以上说法都有可能 |