维生素C是一种水溶性维生素(其水溶液呈酸性),它的化学式是C6H8O6,人体缺乏这样的维生素能得坏血症,所以维生素C又称抗坏血酸。在新鲜的水果、蔬菜、乳制品中都富含维生素C,例如新鲜橙汁中维生素C的含量在500mg/L左右。十二中某研究性学习小组测定了某品牌软包装橙汁中维生素C的含量,下面是他们的实验分析报告。
(一)测定目的:测定×××牌软包装橙汁中维生素C的含量。
(二)测定原理:C6H8O6+I2 →C6H6O6+2H++2I―
(三)实验用品及试剂
(1)仪器和用品(自选,略)
(2)试剂:指示剂_________(填名称,1分),浓度为8.00×10-3mol·L-1的I2标准溶液、蒸馏水等。
(四)实验过程
(3)洗涤仪器,检查滴定管是否漏液,润洗相关仪器后,装好标准碘溶液待用。
(4)用________________(填仪器名称,1分)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂。
(5)用左手控制滴定管的____________(填部位,1分),右手摇动锥形瓶,眼睛注视___________,直到滴定终点。滴定至终点时的现象是________________。
(五)数据记录与处理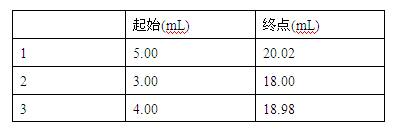
(6)若经数据处理,则此橙汁中维生素C的含量是____________mg/L。
(六)问题讨论
(7)从分析数据看,此软包装橙汁是否是纯天然橙汁?_______(填“是”或“不是”或“可能是”,1分)。生产商最可能采取的做法是__________(填编号,1分):
A.加水稀释天然橙汁 B.将维生素C作为添加剂 C.橙汁已被浓缩
某化学学习小组用如图所示装置研究不同条件下铁与硝酸反应的情况。其实验步骤如下:
①在大试管中先加入一小块铁(过量),再加入一定量的浓硝酸;
②用仪器a再加入适量的水;
③反应结束后取少量上层溶液于另一试管中,滴加几滴KSCN溶液;
④再用仪器a向③的试管中滴加适量的稀盐酸。
请回答下列问题:
(1)仪器a的名称是
(2)步骤①无明显现象,原因是
(3)步骤④的主要现象是
(4)学习小组在进行实验后发现该实验装置存在着一明显的缺陷,请给出一种简单的消除此缺陷的措施。
( 14分)某无色透明溶液可能含有下列离子:K+、Fe3+、Cu2+、Ba2+、AlO、NO3━、CO32-、SO32-、SO42-、Br-、I-、Cl-。取该溶液按如下步骤进行实验。
(1)请你根据下表Ⅰ栏中的实验结果,回答Ⅱ栏中有关问题:
| Ⅰ实验结果 |
Ⅱ回答问题 |
| ①取原溶液少许,滴加足量氯水,产生沉淀;过滤,滤液加CCl4,振荡后,CCl4层未变色。 |
①该步实验说明溶液中不存在离子_________________。 |
| ②取原溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色。 |
②该步实验发生反应的离子方程式为 _________________。 |
| ③取原溶液少许,加盐酸酸化后,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失。 |
③产生白色沉淀的离子方程式为 _________________。 |
| ④取原溶液少许,滴加2滴酸性高锰酸钾溶液,紫色立即褪去。 |
④该步实验说明溶液中存在离子 _________________。 |
| ⑤取原溶液少许,加足量Ba(NO3)2溶液产生白色沉淀,过滤;往洗涤后的沉淀中加入足量盐酸,沉淀部分溶解,有无色气体产生。 |
⑤未溶解的白色沉淀是;将气体通入品红溶液的现象是。 |
| ⑥取步骤⑤所得滤液,加HNO3酸化后,再加AgNO3溶液,溶液中析出白色沉淀。 |
⑥该步骤是否有意义(填“有”或“无”)。 |
(2)综上,该溶液的pH(填“>”、“<”或“=”)7;该溶液中一定存在的阳离子是,不能确定是否存在的离子是;现欲取原溶液检验其是否存在,是否要使用试剂,若不要使用试剂,其实验方法是;若要使用试剂,选用的试剂是(按使用的先后顺序依次写出)
。
Ⅰ某同学帮助水质检测站配制480 mL 0.5 mol/LNaOH溶液以备使用.
(1)该同学应选择 mL的容量瓶.
(2)其操作步骤如乙图所示,则甲图操作应在乙图中的 (填选项字母)之间. 

A.②与③ B.①与② C.④与⑤
(3)该同学应称取NaOH固体 g,用质量为23.1 g的烧杯放在托盘天平上称取所需 NaOH固体时,请在附表中选取所需的砝码大小 (填字母),并在下图中选出能正确表示游码位置的选项 (填字母).
NaOH固体时,请在附表中选取所需的砝码大小 (填字母),并在下图中选出能正确表示游码位置的选项 (填字母).
附表 砝码规格
| a |
b |
c |
d |
e |
|
| 砝码大小/g |
100 |
50 |
20 |
10 |
5 |

(Ⅱ)如图是医院病人输液时用的一瓶质量分数为5%的葡萄糖注射液标签,请认真观察标签上的所列内容后填写:
(1)该溶液中含水 g.
(2)该溶液的密度为 g/mL.
(3)该溶液的物质的量浓度为 mol/L
(3分)乙酸是食醋的主要成分,它具有以下化学性质:‘
(1)可使紫色石蕊试液变______色,说明乙酸具有______性。
(2)能发生酯化反应。实验室用右图所示装置制取乙酸乙酯,请写出该反应的化学方程式:。
(6分) 为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置
(1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”)。
(2)写出制取氨气的化学方程式。
(3)如何检验氨气是否收集满(简述操作方法、现象和结论)。
(4)氨是一种重要的化工产品,其化学式为,具有气味,密度比空气。