滴滴涕(DDT)是20世纪60年代以前广为应用的一种杀虫剂,它可由氯苯制得,其结构简式为 ,因其性质稳定、脂溶性好、药效强、适用性广而大被大量生产,普遍使用,以致最终造成环境污染。为了杀灭对人类有害的昆虫,而又避免或减少环境污染、破坏生态平衡,化学工作者进行了不懈的努力,研制出多种新型杀虫剂,以代替DDT等农药。例如化合物A就是其中一种:
,因其性质稳定、脂溶性好、药效强、适用性广而大被大量生产,普遍使用,以致最终造成环境污染。为了杀灭对人类有害的昆虫,而又避免或减少环境污染、破坏生态平衡,化学工作者进行了不懈的努力,研制出多种新型杀虫剂,以代替DDT等农药。例如化合物A就是其中一种:
请完成下列各题:
(1)化合物A的分子式为________。
(2)化合物A中的官能团有________________(写名称)。
(3)下列对于DDT的说法中错误的是_________。
| A.DDT在杀死害虫的同时,也能杀死有益的生物 |
| B.DDT是一种难溶于水,易溶于有机溶剂的物质 |
| C.DDT的分子式为C14H9Cl5 |
| D.DDT的农药用于蔬菜杀虫时,在蔬菜中残留时间短,对人体无害 |
2012年8月24日,武汉市一家有色金属制造厂发生氨气泄露事故。已知在一定温度下,合成氨工业原料气H2制备涉及下面的两个反应:
C(s)+H2O(g) CO(g)+H2(g);
CO(g)+H2(g);
CO(g)+H2O(g) H2(g)+CO2(g)。
H2(g)+CO2(g)。
(1)判断反应CO(g)+H2O(g) CO2(g)+H2(g)达到化学平衡状态的依据是_____ ___。
CO2(g)+H2(g)达到化学平衡状态的依据是_____ ___。
A.容器内压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(2)在2 L定容密闭容器中通入1 mol N2(g)和3 mol H2(g),发生反应:3H2(g)+N2(g)  2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g),ΔH<0,测得压强-时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
①若图中c=1.6 mol,则改变的条件是________(填字母);
②若图中c<1.6 mol,则改变的条件是_ __(填字母);此时该反应的平衡常数_____(填“增大”、“减小”、“不变”)
A.升温B.降温 C.加压 D.减压 E.加催化剂
(3)如图甲,平衡时氢气的转化率为________。
(4)工业上可利用如下反应:H2O (g)+CH4 (g)  CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如下图所示:0~4 s内,用H2 (g)表示的反应速率为____________,用CO(g)表示的反应速率为__________。
CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如下图所示:0~4 s内,用H2 (g)表示的反应速率为____________,用CO(g)表示的反应速率为__________。
碳、氮、氧、氟都是位于第二周期的重要的非金属元素。请回答下列问题:
(1)基态氟原子的核外电子排布式是______________ 。
(2)C、N、O、F四种元素第一电离能从大到小的顺序是_________________。
(3)①碳和另外三种元素均可形成化合物。四氟化碳的空间构型为____________,CF4可以利用甲烷与Cl2和HF在一定条件下反应来制备,其反应化学方程式为__ __ ___。
②CO是__________分子(填“极性”或“非极性”),CO的常见等电子体为N2、CN-,已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________。
③C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具,可推测出C3N4属于_________晶体。
(4)N4分子结构和白磷一样都是正四面体。又已知断裂1molN-N键吸收167kJ热量,生成1 molN≡N键放出942kJ热量,0.1 molN4转变为N2将放出____________热量:
(5)CaF2和CaC2都属于离子晶体。CaF2晶体的密度为a g·cm-3,则晶胞(如图)的体积是_______________(只要求列出算式)。
(6)CaC2晶体的晶胞与氯化钠相似,但由于CaC2晶体中的C22-存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C22-周围距离最近且相等的Ca2+数目为__________,C22-与O22+互为等电子体,O22+的电子式为____________。
将镁、铝的混合物共0.2 mol, 溶于200 mL 4 mol·L—1的盐酸溶液中,然后再滴加2mol·L—1的NaOH溶液。请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示。当V1="160" mL时,则金属粉末中n (Al)=mol;
(2)0~V1段发生的反应的离子方程式为;
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+ 刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=mL;
(4)若镁、铝的混合物仍为0.2 mol,其中镁粉的物质的量分数为a,改用200 mL 4mol·L—1的硫酸溶解此混合物后,再加入840mL 2 mol·L—1的NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为。
下列框图所示的转化关系中,A、C均为常见的金属单质,A、C在冷的H的浓溶液中均会发生钝化;E为固体非金属单质。B为红色固体氧化物,X为常见的无色液体。L焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)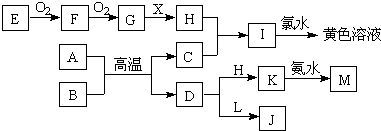
请回答以下问题:
(1)含碳量在0.03 %~2 %之间的C的合金,是目前世界上使用量最大的合金,这种合金是;
A.铝合金B.青铜C.镁合金D.钢铁
(2)F的化学式为;
(3)I与氯气反应的离子方程式为;
(4)A与B生成C和D的反应是(填“放出”或“吸收”)大量热量的反应;
(5)D与L反应的离子方程式为。
某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题: 
(1)沉淀A的成分是(填化学式),沉淀B的成分是(填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为:、 ;
(3)在操作Ⅰ的名称是,其中玻璃棒的作用是。