乙烯是石油裂解的主要产物之一。将乙烯通入溴的四氯化碳溶液中,观察到的现象是________________;其反应方程式为________________。乙烯在一定条件下发生加聚反应的化学方程式是________,其产物的名称是________;乙烯对水果具有________功能。
. 用双线桥法表示下列化学反应中的电子转移情况,是离子反应的将其改写为离子方程式,不是离子反应的可不填.
(1) 加热硝酸铵
5NH4NO3 4N2↑+2HNO3+9H2O
4N2↑+2HNO3+9H2O
(2)在含有Na2S和Na2SO3的溶液中,加入稀硫酸
2Na2S+Na2SO3+3H2SO4==3Na2SO4+3S↓+3H2O
(3)铜片与稀硝酸反应
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO+4H2O
(12分)氯化钠溶液在生产、生活中都有广泛的用途。现配置1 L 0.2 mol·L-1 NaCl溶液。请回答问题。
| 实验步骤 |
有关问题 |
| (1)计算并称量 |
需要NaCl的质量为________g |
| (2)溶解 |
为加速溶解,可进行的操作是________ |
(3)转移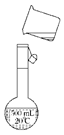 |
a. 指出示意图中的两处错误:错误1: _____________________ ________________________ ________________________ ____ ____错误2:___________________________________________ b. 若容量瓶不干燥,含有少量蒸馏水,会造成所配溶液的物质的量浓度 (填“偏高”“偏低”或“无影响”) |
| (4)定容 |
若仰视容量瓶刻度线,定容后会造成所配溶液的物质的量浓度________(填“偏高”“偏低”或“无影响”) |
已知X溶液有如图所示转化关系: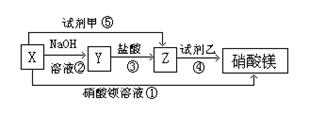
(1)根据上述转化关系,写出下列物质的化学式:X、Y、Z、试剂甲,试剂乙。
(2)写出上述各步反应①~④的离子方程式:
①;②;
③;④ 。
(9分)①在进行过滤操作时,需用到的玻璃仪器是
②在进行分液和配制物质的量浓度溶液时,首先要分别对分液漏斗、容量瓶进行 .
③用一种试剂除去NaCl溶液中含有的CuCl2,写出所用试剂及反应的离子方程式
除杂试剂: (写化学式)离子方程式:
根据下列框图关系填空。已知常温下X为无色液体,D、E均为无色气体,
G是一种主要的工 业产品。C的焰色反应为黄色,E、F的相对分子量之间的关系为
业产品。C的焰色反应为黄色,E、F的相对分子量之间的关系为
M(F)=M(E)+16。回答下列问题: 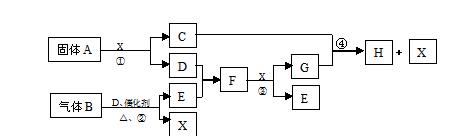
(1)A中化学键的类型为,写出B的一个用途。
(2)将固体A加入CuSO4溶液中的主要现象是 。
。
(3)写出气体B的水溶液与CuSO4溶液反应的离子方程式。
(4)写出反应②的化学方程式,若是氧化还原反应,请标出电子转移的方向和数目。
(5)经测定,反应④中每生成1.0gX,放出3.2KJ的热量(常温下)。试写出反应④的热化学方程式。