用脱脂棉包住约0.2g过氧化钠固体粉末,置于石棉网上,然后向包有过氧化钠的位置滴加几滴水,结果脱脂棉剧烈燃烧起来。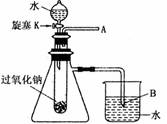
试完成下列问题:
(1)写出过氧化钠与水反应的化学方程式
(2)结合脱脂棉剧烈燃烧的实验事实及燃烧的条件可以得出的结论是
(3)某研究性学习小组,为进一步证明上述结论,拟用如图所示的装置进行有关实验。请写出有关的实验操作方法
现象:A处: B处:
三苯甲醇( )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示。
已知:i)格氏试剂容易水解,
ii)相关物质的物理性质如下:
| 物质 |
熔点(℃) |
沸点(℃) |
溶解性 |
| 三苯甲醇 |
164.2 |
380 |
不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 |
—116.3 |
34.6 |
微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 |
—30.7 |
156.2 |
不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 |
—34.6 |
212.6 |
不溶于水 |
| Mg(OH)Br |
常温下为固体 |
能溶于水,不溶于醇、醚等有机溶剂 |
iii)三苯甲醇的相对分子质量是260,纯净固体有机物一般都有固定熔点。
请回答以下问题:
(1)实验室合成三苯甲醇的装置图2,写出玻璃仪器A的名称:,装有无水CaCl2的仪器A的作用是:;
(2)制取格氏试剂时要保持微沸,可以采用水浴加热,优点是,微沸回流时冷凝管中水流的方向是:(填“X→Y”或“Y→X”);
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写空白:
其中,操作①为:;洗涤液最好选用:;
A.水 B.乙醚 C.乙醇 D.苯
检验产品已经洗涤干净的操作为:;
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80m L(标准状况)。产品中三苯甲醇质量分数为(保留两位有效数字,已知三苯甲醇的分子式为C19H16O,相对分子质量为260)。
某兴趣小组根据镁与沸水的反应推测镁也能与饱和碳酸氢钠溶液反应。资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。该兴趣小组设计了如下实验方案并验证产物、探究反应原理。
实验1:用砂纸擦去镁条表面氧化膜,将其放人盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
(1)提出假设
该同学对反应中产生的白色不溶物作出如下假设:
假设1:可能为。
假设2:可能为MgCO3。
假设3:可能是碱式碳酸镁[xMgCO3·yMg(OH)2]
(2)设计定性实验确定产物并验证猜测:
| 实验序号 |
实验 |
预期现象和结论 |
| 实验II |
将实验I中收集到的气体点燃 |
|
| 实验III |
取实验I中的白色不溶物,洗涤,加入足量 |
; 白色不溶物可能含有MgCO3 |
| 实验IV |
取实验I中的澄清液,向其中加入少量CaCl2稀溶液 |
产生白色沉淀;溶液中存在离子 |
(3)设计定量实验确定实验I的产物:称取实验I中所得干燥、纯净的白色不溶物31.0 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入盛有足量浓硫酸的洗气瓶A、盛有足量碱石灰的干燥管B和盛有足量碱石灰的干燥管C中。实验前后装置A增重1.8 g,装置B增重13.2 g,试确定白色不溶物的化学式。
(4)请结合化学用语和化学平衡移动原理解释Mg和NaHCO3溶液反应产生大量气泡的原因。
Ba(NO3)2可用于生产绿色烟花、绿色信号弹、炸药等。某生产BaCO3、BaSO4的化工厂生产中排出大量的钡泥[主要含有BaCO3、BaSO3、Ba(FeO2)2等],该厂利用钡泥制取Ba(NO3)2晶体(不含结晶水),其部分工艺流程如下: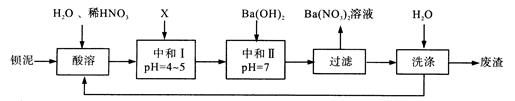
已知: ①Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7;
②Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9。
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式说明提纯原理:。
(2)酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为。
(3)该厂结合本厂实际,选用的X为(填序号),中和I使溶液中的(填离子符号)的浓度减小。
| A.BaCl2 | B.Ba(OH)2 | C.Ba(NO3)2 | D.BaCO3 |
(4)最后的废渣中除原有的难溶性杂质外还含有(填化学式)。
(5)测定所得Ba(NO3)2晶体的纯度:准确称取m1g晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m2g,则该晶体纯度的计算表达式为。(已知Ba(NO3)2、BaSO4的式量分别为261、233)
二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色的气体,易溶于水。实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料来制备ClO2,其流程如下:
(1)写出电解时发生反应的化学方程式:。
(2)除去ClO2中的NH3可选用的试剂是。(填字母)
| A.饱和食盐水 | B.碱石灰 | C.浓硫酸 | D.水 |
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去VmL硫代硫酸钠溶液。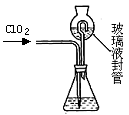
①装置中玻璃液封管的作用是;。
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式 。
③滴定终点的现象是:。
④测得通入ClO2的质量m(ClO2)=。(用含c、V的代数式表示)(已知:ClO2的相对分子质量为67.5)
(4)设计实验来确定溶液X的成分,请补充完成实验步骤和现象。
| 实验步骤 |
实验现象 |
实验结论 |
| ① |
溶液X中含有Na+ |
|
| ② |
溶液X中含有Cl- |
高铁酸钾广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如下: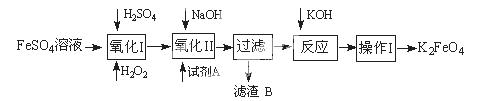
查资料得知K2FeO4的一些性质:
①在碱性环境中稳定,在中性和酸性条件下不稳定
②溶解度很大,难溶于无水乙醇等有机溶剂
③具有强氧化性,能氧化有机烃、苯胺和80%以下乙醇溶液
回答下列问题:
(1)写出“氧化I”中,生成Fe3+的离子反应方程式。
(2)氧化II中,试剂A为 (填“H2O2”或“HNO3”或“NaClO”);过滤操作中,得到的滤渣B中除NaCl还有
(3)操作I中包括冷却结晶、过滤、洗涤干燥几个步骤。洗涤干燥的目的是脱碱脱水,进行该操作时最好用洗涤。
(4)净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式:K2FeO4 + H2O = Fe(OH)3↓ + KOH +
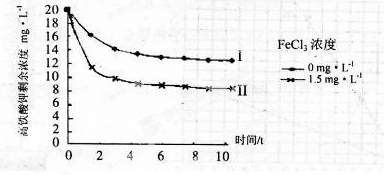
(5)将一定量的K2FeO4投入一定浓度的FeCl3溶液中,测得剩余K2FeO4浓度如下图所示,推测产生曲线I和曲线II差异的原因是。