(1)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,溶液中c(CH3COO-) c(Na+)。(填大于、小于、等于)
(2)将pH=3的硫酸溶液和pH=12的氢氧化钠溶液混和,若使混和后溶液的pH=7,则硫酸溶液和氢氧化钠溶液的体积比是_______
(3)某酸性化工废水中含有浓度约为0.01mol.L-1的Ag+、Pb2+等重金属离子。有关数据如下:
| 难溶电解质 |
AgI |
AgOH |
Ag2S |
PbI2 |
Pb(OH)2 |
PbS |
| Ksp |
8.3×10-12 |
5.6×10-8 |
6.3×10-50 |
7.1×10-9 |
1.2×10-15 |
3.4×10-28 |
(i)在废水排放前,用沉淀法除去这两种离子, 最好加入_________(填字母序号)
A. Na2S、 B. NaOH 、 C.KI、 D.Ca(OH)2
(ii)某工程师用CaO处理上述废水后Pb2+的浓度为1.2×10-3 则此溶液的pH=____。
将一段乳胶管放到汽油中浸泡一段时间,可观察到的现象是____________________,其原因是____________________,由此可知,一般的橡胶制品在使用时不宜与____________________直接接触。
下列反应中
①2KClO3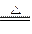 2KCl+3O2↑
2KCl+3O2↑
②C+CO2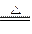 2CO
2CO
③HgS+O2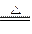 Hg+SO2
Hg+SO2
④2KMnO4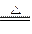 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
⑤2KNO3 2KNO2+O2↑
2KNO2+O2↑
⑥Cl2+H2O====HClO+HCl
(1)属于一种元素还原两种元素的是__________。
(2)属于同种元素间氧化还原反应的是__________。
下图中各图象表示N2(g)+3H2(g) 2NH3(g)(正反应为放热反应)达到平衡后,只改变一个条件时建立的新平衡的过程。填写下列各空(均填写图序号):
2NH3(g)(正反应为放热反应)达到平衡后,只改变一个条件时建立的新平衡的过程。填写下列各空(均填写图序号):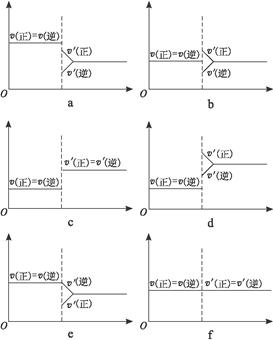
(1)表示减少H2而建立新的平衡的是图_______________;
(2)表示压缩气体体积后建立新的平衡的是图_______________;
(3)表示降低温度而建立新的平衡的是图_______________;
(4)表示体积不变充入N2、H2,同时分离出NH3建立新的平衡的是图_______________;
(5)表示加入催化剂建立新的平衡的是图_______________;
(6)表示充入氩气(体积不变)后,建立新的平衡的是图_______________。
在一个固定体积的密闭容器中加入2 mol A和1 mol B,发生如下反应:
2A(g)+B(g) 3C(g)+D(g)
3C(g)+D(g)
达到平衡时,C的浓度为w mol·L-1。若维持容器体积和温度不变,用下列物质作为起始物质时,经反应达平衡后C的浓度(填“大于”“小于”或“等于”):
(1)加入1 mol A和1 mol B时,C的平衡浓度___________________________w mol·L-1。
(2)加入2 mol A和1 mol B,3 mol C和1 mol D时,C的平衡浓度___________w mol·L-1。
(3)加入3 mol C和1 mol D时,C的平衡浓度_____________________________w mol·L-1。
(4)加入2 mol B、3 mol C、1 mol D时,C的平衡浓度_____________________w mol·L-1。
(4分)常温下,浓度均为0.1 mol·L-1的①NaHCO3②NaClO③NH4Cl④NaCl⑤Na2CO3五种溶液的pH由大到小的顺序是___________。