下列为A、B、C、D四种物质的转化关系,a、b为反应条件,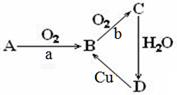
(1)若A为单质,a为点燃,b为催化剂、加热,
① D的化学式为
② 写出B到C的化学方程式 。
(2)若A为气态化合物,a为催化剂、加热,B到C转化不需要条件,
①写出C→D化学方程式 。②写出Cu与D的稀溶液反应的离子方程式 。
敌草胺是一种除草剂。它的合成路线如下:

回答下列问题:
(1)在空 气中久置,
由无色转变为棕色,其原因是。
气中久置,
由无色转变为棕色,其原因是。
(2)
分子中有2个含氧官能团,分别为和填官能团名称)。
(3)写出同时满足下列条件的
的一种同分异构体的结构简式:。
①能与金属钠反应放出
;②是萘( )的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氧。
)的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氧。
(4)若
不经提纯,产物敌草胺中将混有少量副产物
(分子式为
),
是一种酯。
的结构简式为。
(5)已知: ,写出以苯酚和乙醇为原料制备
,写出以苯酚和乙醇为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图例如下:
以硫铁矿(主要成分为
)为原料制备氯化铁晶体(
)的工艺流程如下:
回答下列问题:
(1)在一定条件下,
转化为
 的反应为
,该反应的平衡常数表达式为
=;过量的
与
溶液反应的化学方程式为
的反应为
,该反应的平衡常数表达式为
=;过量的
与
溶液反应的化学方程式为
(2)酸溶及后续过程中均需保持盐酸过量,其目的是、。
(3)通氯气氧化后时,发生的主要反应的离子方程式为;该过程产生的为其可用碱溶液吸收,为其中污染空气的气体为(写化学)。
美国化学家
因发现如下
反应而获得2010年诺贝尔化学奖。 (
为卤原子,
为取代基)
(
为卤原子,
为取代基)
经由
反应合成
(一种防晒剂)的路线如下:
回答下列问题:
(1)
可发生的反应类型是。
a.取代反应 b.酯化反应
c.缩聚反应 d.加成反应
(2)
与浓
共热生成
,
能使酸性
溶液褪色,
的结构简式是。
在一定条件下反应生成高分子化合物
,
的结构简式是。
(3)在
的反应中,检验
是否反应完全的试剂是。
(4)
的一种同分异构体
符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与
溶液作用显紫色。
与过量
溶液共热,发生反应的方程式为。
氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为个.
(2)
分子内的
键、分子间的范德华力和氢键从强到弱依次为。 沸点比
沸点比 高,原因是.
高,原因是.
(3)
可与
形成
,
中
原子采用杂化。
中
键角比
中
键角大,原因为。
(4)
与
的晶胞同为面心立方结构,已知
晶体密度为ag cm-3,
表示阿伏加德罗常数,则
晶胞体积为Cm3。
cm-3,
表示阿伏加德罗常数,则
晶胞体积为Cm3。
水处理技术在生产、生活中应用广泛。
(1)含有较多离子的水称为硬水。硬水加热后产生碳酸盐沉淀的离子方程式为写出一个即可)。
(2)将
型阳离子交换树脂和
型阴离子交换树脂串接来软化天然硬水,应先使硬水通过(填"
"或"
")型离子交换树脂,原因是。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为。电渗析法净化水时,使离子通过半透膜的推动力是。
(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的。