配平下列各氧化还原反应方程式(将系数填写在相应横线上,并按要求填空)
⑴ ___ KMnO4 + ___ HCl =" _____" MnCl2 + _____ KCl + ____ Cl2 ↑ + ___ H2O
⑵ ____ HNO3 = ___NO2 ↑ + _____ O2 ↑+ _____H2O
⑶ _____Na +____Cu2+ + ____H2O ==______Na+ + ____Cu(OH)2 ↓ + ____H2 ↑
该反应的氧化剂是 ;若转移的电子数是1mol,则得到H2 mol
25℃、1.01×105Pa时,氢硫酸饱和溶液的浓度为0.1mol·L-1,氢硫酸溶液呈酸性,用方程式表示主要原因。向溶液中加入少量Na2S晶体,振荡后溶液的pH将(填“增大”、“减小”或“不变”)。
选择下列实验方法分离物质,将分离方法的序号填在横线上。
A、分液法 B、加热分解 C、结晶法 D、分液法 E、蒸馏法 F、过滤法
(1)分离饱和食盐水和沙子的混合物
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾
(3)分离水和汽油的混合物
(4)分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),已知四氯化碳和甲苯互溶
用图所示的装置进行电解。通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。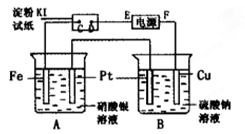
(1)E为电源的极(填“正”或“负”);
(2)A中发生反应的化学方程式为;
(3)在B中观察到的现象是;
(4)室温下,若从电解开始到结束,A、B装置中共 收集到气体0.168 L(标况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求A溶液的pH。
收集到气体0.168 L(标况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求A溶液的pH。
某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及 电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如下图所示,回答下列问题:
电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如下图所示,回答下列问题: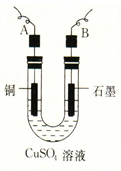
(1)该装置中B电极为电解池的极(填“阴”或“阳”);
(2)A电极上的电极反应式为;
电解池总反应的离子方程式为;
(3)电解过程中,电解质溶液的酸性(填“增强”、“减弱”或“不变”);
(4)下列实验操作中必要的是(填写字母);
| A.称量电解前的电极的质量; |
| B.电解后,电极在烘干称量前,必须用蒸馏水冲洗; |
| C.刮下电解后电极上析出的铜,并清洗,称量; |
D.电解后烘干称重的操作中必须按“烘干→称量 →再烘干→再称量”进行; →再烘干→再称量”进行; |
(E)在有空气存在的情况下,烘干电极必须用低温烘干的方法。
(5)铜的相对原子质量为(用带有m、V的计算式表示)。
为减弱温室效应,除了减少CO2的排放、植树造林、将液态CO2注入深海等措施外,还有一种思路是将CO2转化成其它可燃物质。如工业上已实现CO2和H2反应生成甲醇的转化。已知:在一恒温、恒容密闭容器中充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) =CH3OH(g)+H2O(g)


 △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答
△H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答 :
: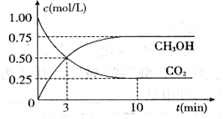
(1)达到平衡的时刻是____________min(填“3”或“10”)。 在前10min内,用CO2表示的反应速率
在前10min内,用CO2表示的反应速率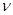 (CO2)="________"
(CO2)="________"
(2)能判断该反应达到化学平衡状态的依据是。 a.容器压强不变 b.混合气体中c(CO2)不变
a.容器压强不变 b.混合气体中c(CO2)不变
c.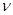 (CH3OH)=
(CH3OH)= 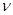 (H2O) d.c(CH3
(H2O) d.c(CH3 OH)=c(H2O)
OH)=c(H2O) (3)为了提高H2的转化率,可采取__________(填“增大”或“减小”)CO2浓度的措施。
(3)为了提高H2的转化率,可采取__________(填“增大”或“减小”)CO2浓度的措施。
(4)达平衡后,H2的转化率是_____________。平衡常数K=____________。(计算结果保留一位小数)