氧化还原反应在工农业生产和日常生活中有广泛运用。
(1)罐头厂在装食物罐头时通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类防腐剂应具有 。(填“氧化性”或“还原性”);
(2)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是 。(填“氧化作用”或“还原作用”);
(3)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。
(4)在下列的空白处填写最适宜的除杂试剂,并写出相应的离子方程式
①FeCl2中含少量FeCl3杂质 , 。
②FeCl3中含少量FeCl2杂质 , 。
③FeSO4中含少量CuSO4 杂质 , 。
某同学运用已有的Na2O2和CO2反应的知识进行迁移,认为Na2O2也可和SO2反应,反应式可能为:2Na2O2+2SO2=====2Na2SO3+O2,为此设计如下一套装置,来验证Na2O2和SO2的反应产物。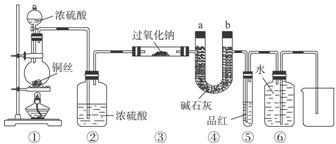
如图安装仪器,检查装置气密性后添加药品并滴入适量浓硫酸。完成下列问题:
(1)点燃①处酒精灯,不久,观察到①处产生大量气体;③处硬质玻璃管的管壁发热,管内药品的颜色变化为由___________色逐渐变为___________色。
(2)在反应过程中如何用较简便的操作证明反应产生了O2?
_______________________________________________________________________________。
(3)⑥处用排水法收集气体,从什么现象可证明收集的气体中已不含SO2?
_______________________________________________________________________________。
(4)待反应结束后,取硬质玻璃管内少量固体,装入试管中,加水溶解时未产生气体,如何证明产物中有Na2SO3?
_______________________________________________________________________________。
(5)待反应结束后,取硬质玻璃管内少量固体,装入试管中,加入足量盐酸溶液,无气体放出,再加入氯化钡溶液,有白色沉淀生成,试分析产生沉淀的原因______________________。
已知A、B、C、D、E是短周期原子序数依次增大的五种元素。且原子半径C>D>E>A>B,A、E同主族,A、B、E的原子序数之和与D元素最高价氧化物对应水化物中的电子总数相等,且最高价氧化物对应水化物中的电子数C、D之和与E相等。试推断:
(1)A_____________,B_____________,C_____________,D_____________,E_____________(填元素符号)。
(2)写出C单质在空气中燃烧产物的电子式__________________________。
(3)同周期元素中最高价氧化物对应水化物电子总数与E相等的还有_____________、_____________。(填元素符号,至少填两个)
(4)写出由A、D两元素形成的化合物与水反应的化学反应方程式____________________
_____________________________________________________________________。
未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机。这类材料中研究得较多的是化合物G。
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:①化合物G的化学式为__________________。②由1 mol NH3和0.75 mol E恰好完全反应,化合物E的分子式为_______________________。
(2)粉末状G能够与空气中的氧气和水作用,所得产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料。与氧反应所得的产物还有一种单质;与水反应生成另一种产物是该种单质元素的氢化物。请写出化合物G与水反应的化学方程式_______________________________________________________________________________。
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-xAlxOxY8-x。在接近于1 700 ℃时x的极限值约为4.0,在1 400 ℃时x为2.0,以保持整个化合物呈电中性。试问:①赛伦中各元素的化合价为Si_________,Al_________,O_________,Y_________。赛伦的晶体类型为_________。
下图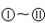 分别代表有关反应中的一种物质,请填下以下空白。
分别代表有关反应中的一种物质,请填下以下空白。
(1)①、③、④的化学式分别是、、。
(2)⑧与⑨反应的化学方程式是。
A、B、C是在中学化学中常见的三种化合物,它们各由两种无素组成,甲、乙是两种单质。这些化合物和单质之间存在如下的关系: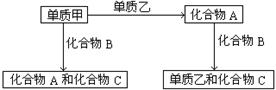
据此判断:(1)在A、B、C这三种化合物中,必定含有乙元素的是 (用A、B、C字母填写)。
(2)单质乙必定是 (填“金属”或“非金属”),其理由是 。
(3)单质乙的化学式可能是 ,则化合物B的化学式是 。