已知反应A2(g)+2B2(g) 2AB(g)的△H<0,下列说法正确的是
2AB(g)的△H<0,下列说法正确的是
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
据报道,我国拥有完全自主产权的氢氧燃料电池车将在奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是()
| A.正极反应式为:O2+2H2O+4e-="===" 4OH- |
| B.工作一段时间后,电解液中的KOH的物质的量不变 |
| C.负极反应式为:H2-2e-===2H+ |
| D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.2mol电子转移 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiO(OH) + 2H2O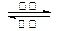
 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是()
| A.充电时阳极反应:Ni(OH)2 + OH- -e-="=" NiO(OH )+ H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
反应2A(g) 2B(g)+C(g)是放热反应,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是()
2B(g)+C(g)是放热反应,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是() A.升温 B.增大反应器的体积 C.增大c(A) D.降温
A.升温 B.增大反应器的体积 C.增大c(A) D.降温
已建立化学平衡的某可逆反应,当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是()
①生成物的质量分数一定增加
②任一生成物总量一定增加
③反应物的转化率一定增大
④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率
⑥一定使用催化剂
| A.①②③ | B.③④⑤ | C.②⑤ | D.④⑥ |
下列说法正确的是()
| A.凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
B.自发 反应一定是熵增大,非自发反应一定是熵减小或不变 反应一定是熵增大,非自发反应一定是熵减小或不变 |
| C.自发反应在恰当的条件下才能实现 |
| D.自发反应在任何条件下都能实现 |