t℃时,将3molA和1molB气体通入体积为2L的密闭容器中(恒容),发生如下反应:
3A(g)+ B(g )  xC(g),2min 时反应达到平衡状态(温度保持不变),剩余0.8 molB,C的浓度为0.4mol·L-1,请填空:
xC(g),2min 时反应达到平衡状态(温度保持不变),剩余0.8 molB,C的浓度为0.4mol·L-1,请填空:
⑴从开始反应至达到平衡状态,以B表示的平均反应速率为
⑵x=
⑶若继续向原平衡混合物的容器中通入适量氦气(假设氦气和A、B、C都不反应)后,原化学平衡________(填字母)
A.向正反应方向移动 B.向逆反应方向移动 C.不移动 D.无法判断
⑷若向原平衡混合物的容器中再充入3molA和1molB,在t℃时达到新的平衡,此时B的物质的量为n(B)______1.6mol。(填“>”、“<”、或“=”)
⑸如果将amolA、bmolB、cmolC在相同温度和容器中进行反应,欲使反应达到平衡时C的物质的量浓度分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的等量关系式:__________________、__________________(a与c及b及c的关系式)
(1)常压、100℃时,等质量的SO2气体和SO3气体的密度之比为 ,原子数之比为 ,体积之比
(2)有CO与CO2的混合气体共10.8 g,标准状况下其体积为6.72L。则混合气体中二氧化碳的物质的量为 ,若混合气体缓慢通过足量的氢氧化钠溶液后,剩余的气体质量为 。
(3)将0.1 mol·L-1的K2SO4溶液、0.2 mol·L-1的Al2(SO4)3溶液和纯水混合,要使混合液中K+、Al3+、SO42-的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,求K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比 。(忽略体积的变化)
在0.4 L由NaCl 、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。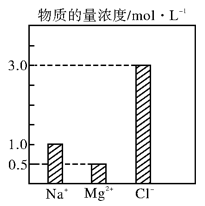
(1)该混合液中,NaCl的物质的量为____________mol,含溶质MgCl2的质量为______________g。
(2)该混合液中CaCl2的物质的量为____________mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为______________mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀____________mol。
(1)18.4 g氮的氧化物N2Ox中含氮原子0.4 mol,则N2Ox的摩尔质量为 ;x= ;
(2)设一个12C原子的质量为a g,一个R原子的质量为b g,阿伏加德罗常数的值为NA,则R的相对原子质量可以表示为__________________
(3)标准状况下,224L的NH3溶于680 ml水中,所得溶液的溶质质量分数为 ,若该溶液的密度为 a g/cm3,则其物质的量浓度为 mol·L-1。将上述氨水全部转化为NH4Cl,所需2 mol/L的盐酸的体积为 L(已知:NH3+HCl=NH4Cl)
在①渗析 ②聚沉 ③溶胶 ④凝胶 ⑤布朗运动 ⑥电泳 ⑦丁达尔现象 ⑧中和 ⑨水解中选出适宜的词语填入下列每小题的空格中(填编号):
(1)肥皂水中透过强光,可以见到光带。这种现象称为_____________________。
(2)在氢氧化铁胶体中加入硫酸,先产生红褐色沉淀后沉淀溶解,这种现象叫做___________________。
(3)用半透膜把制取的氢氧化铁胶体中含有的NaCl分离出来的方法叫做___________________。
在 1.0L恒容密闭容器中放入0.10 mol A (g),在一定温度进行如下反应。A(g) 2B(g)+ C(g)+ D(s)△H=" +" 85.1 kJ / mol
2B(g)+ C(g)+ D(s)△H=" +" 85.1 kJ / mol
容器内气体总压强(P)与起始压强P。的比值随反应时间(t)变化数据见下表(提示:密闭容器中的压强比等 于气体物质的量之比)。
| 时间t/min |
0 |
1 |
2 |
4 |
8 |
16 |
20 |
25 |
| P/P0 |
1.00 |
1.50 |
1.80 |
2.20 |
2.30 |
2.38 |
2.40 |
2.40 |
回答下列问题:
(1)下列能提高 A 的转化率的是 。
A.升高温度 B.向体系中通人A气体
C.减少D的物质的量 D.向体系中通人稀有气体He
(2)反应进行1小时,容器中剩余A的物质的量为 mol。
(3)平衡时A的转化率为
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则 D 的取值范围n(D)mol。
(5)将容器改为恒压容器,改变条件,使反应达到相同的限度,则达到平衡时B的浓度为 。