(1)18.4 g氮的氧化物N2Ox中含氮原子0.4 mol,则N2Ox的摩尔质量为 ;x= ;
(2)设一个12C原子的质量为a g,一个R原子的质量为b g,阿伏加德罗常数的值为NA,则R的相对原子质量可以表示为__________________
(3)标准状况下,224L的NH3溶于680 ml水中,所得溶液的溶质质量分数为 ,若该溶液的密度为 a g/cm3,则其物质的量浓度为 mol·L-1。将上述氨水全部转化为NH4Cl,所需2 mol/L的盐酸的体积为 L(已知:NH3+HCl=NH4Cl)
如图所示,在一个小烧杯里加入研细的20g Ba(OH)2·8H2O晶体。
将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入10g NH4Cl晶体,并用玻璃棒快速搅拌。实验中要用玻璃棒搅拌的原因是___________________。
(2)写出有关反应的化学方程式:___________________,该反应___________(填“是”或“不是”)氧化还原反应。
(3)该实验中观察到的现象除产生刺激性气味的气体及反应混合物呈糊状以外,还有____________________________________________ 。
(4)通过最后一个现象可以说明该反应为__________(填“吸”或“放”)热反应,这是由于反应物的总能量_______(填“大于”或“小于”)生成物的总能量。
下图是A~ O 的转化关系。已知A是一种金属单质,B、C、D、E、F、H、I、J、K常温常压下均为气体,且B、C、D、E是单质,I是一种红棕色气体,G是一种淡黄色固体,M是混合物,含有气体,J与K相遇会产生大量白烟。请回答下列问题:
(1)写出G与水反应的化学方程式;写出气体E与N溶液反应的离子方程式。
(2)化合物G中含有的化学键为。
(3)写出F的电子式,化合物O的电子式。
(4)E与F反应生成气体的化学方程式为。
(10分(1)和(3)各3分其余每空2分)下图是甲、乙两位同学探究铜与稀硝酸反应还原产物的实验装置图,请图回答下列问题: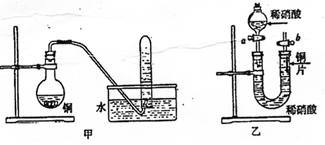
(1)写出铜和稀硝酸反应的离子方程式 。
(2)实验装置甲能否证明铜和稀硝酸反应的产物是NO气体 (填:“能”或“不能”)请阐述理由(包括化学方程式)是
(3)若用实验装置乙进行实验,检查装置气密性的操作是
苯佐卡因是一种局部麻醉剂,可用于粘膜溃疡、创面及痔疮的镇痛,一般制成软膏或栓剂合用。其合成路线如下图所示,其中有机物B具有酸性。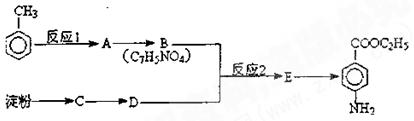
已知:①苯环上的取代反应有如下定位规律:当苯环上的碳原子连有甲基时,可在其邻位或对位上引入官能团;当苯环上的碳原子连有羧基时,可在其间位上引入官能团;
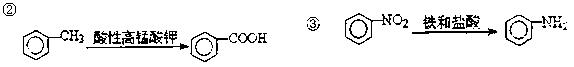
(1)反应类型:反应1 ;反应2 ;
(2)化合物A、C的结构简式:A ;C ;
(3)写出下列转化的化学方程式
C→D:
B+D→E:
(4)苯莽卡因有多种同分异构体,其中氨基直接连在苯环上,分子结构中含有-COOR官能团,且苯环上的一氯代物只有两种的同分异构体共有六种,除苯佐卡因外,其中三种的结构简式为: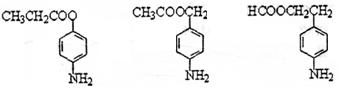
则剩余两种同分异构体的结构简式为: 、 。
实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜 色发生变化所用去的时间来判断空气中的含汞量,其反应为:
色发生变化所用去的时间来判断空气中的含汞量,其反应为:
4CuI+Hg==Cu2HgI4+2Cu、
(1)上述反应产物Cu2HgI4中,Cu元素显 价。
(2)以上反应中的氧化剂为 ,当有1molCuI参与反应时,转移电子 mol。