某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是( )
| A.溶液A和B均可以是盐酸或NaOH溶液 |
| B.若溶液B选用浓硝酸,则测得铜的质量分数偏小 |
| C.溶液A和B均可选用稀硝酸 |
| D.实验室中方案Ⅱ更便于实施 |
某温度下在容积为2 L的密闭容器中,发生2X(g)+Y(g) 2W(g)的反应,当充入1 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是
2W(g)的反应,当充入1 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是
| A.若升高温度,W的体积分数减小,则该反应ΔH<0 |
| B.以Y的浓度变化表示的反应速率为0.01 mol/(L·s) |
| C.在其他条件不变的情况下,增加1 mol X,则X和Y的转化率均提高 |
| D.增大压强正反应速率增大,逆反应速率减小,则平衡向正反应方向移动 |
在密闭容器中,反应X2(g)+Y2(g) 2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是
2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是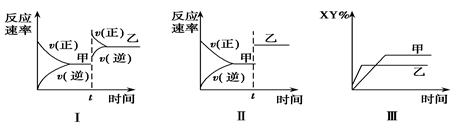
| A.图Ⅰ是增大压强的变化情况 |
| B.图Ⅱ是一定是加入催化剂的变化情况 |
| C.图Ⅲ是增大压强或升高温度的变化情况 |
| D.图Ⅲ一定是升高温度的变化情况 |
反应N2(g)+3H2(g) 2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是
2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是
| A.t0~t1 | B.t2~t3 | C.t3~t4 | D.t5~t6 |
对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是
①生成物的百分含量一定增加 ②生成物的产量一定增加
③反应物的转化率一定增大 ④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率 ⑥使用了适宜的催化剂
| A.②⑤ | B.①② | C.③⑤ | D.④⑥ |
用铁片与稀硫酸反应制取氢气时,下列措施可以使氢气生成速率加大的是
| A.加入少量的硫酸钠 | B.加入硝酸钠固体 |
| C.滴加少量CuSO4溶液 | D.改用浓硫酸 |