地壳中含量第一和第二的两种元素所形成的化合物不具有的性质是( )
A﹒熔点很高 B﹒与水反应生成对应的酸
C﹒可与烧碱反应生成盐 D﹒坚硬
将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3= 9Fe(NO3)x+ NO↑ +14H2O,下列判断合理的是
| A.Fe(NO3)x中的x为2 |
| B.稀HNO3在反应中只表现氧化性 |
| C.磁性氧化铁中的所有铁元素全部被氧化 |
| D.反应中每还原0.3mol氧化剂,就有0.9mol电子转移 |
下列有关说法正确的是
A.含有大量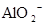 的溶液中:K+、 的溶液中:K+、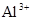 、 、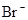 、 、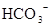 可共存 可共存 |
B.CO(g)的燃烧热是283.0kJ·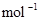 ,则 ,则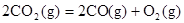 反应的 反应的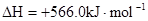 |
| C.用NaOH溶液雕刻工艺玻璃上的纹饰 |
D.在某钠盐溶液中含有等物质的量的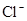 、 、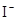 、 、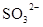 、 、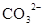 、 、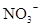 、 、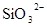 中一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有 中一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有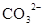 |
在常温常压下,向100mLCH4和Ar的混合气体中通入400mLO2,点燃使其完全反应,最后在相同条件下得到干燥气体450mL,则反应前混合气体中CH4和Ar的物质的量之比为
| A.1:4 | B.1:3 | C.1:2 | D.1:1 |
正确表示下列反应的离子反应方程式为
A.NH4HCO3溶于过量的浓KOH溶液中并加热:NH4++ HCO3-+2OH-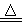 CO32-+ NH3↑+2 H2O CO32-+ NH3↑+2 H2O |
| B.Fe溶于硝酸:Fe+2H+﹦Fe2++H2↑ |
| C.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ |
| D.醋酸除去水垢:2H++CaCO3=Ca2++ CO2↑+ H2O |
下列实验不能达到预期目的的是
| 序号 |
实验操作 |
实验目的 |
| A |
浓、稀HNO3分别与Cu反应 |
比较浓、稀HNO3的氧化性强弱 |
| B |
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 |
说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C |
测定等浓度的HCl、HNO3两溶液的pH |
比较Cl、N的非金属性强弱 |
| D |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究浓度对反应速率的影响 |