A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。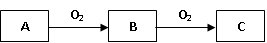
(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,C可用在矿山、坑道、潜水或宇宙飞船等缺氧的场合,将人们呼出的CO2再转换成O2,以供呼吸之用,请用化学方程式表示该反应原理 。
(3)若A为能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体,且B和C易在空气形成光化学烟雾。
①则A为 ,C为 ,(填写化学式)
实验室用熟石灰与氯化铵固体共热制取A,写出此化学方程式: 。
②写出C与水反应的化学方程式: 。
《化学反应原理》一书中,我们学习了两个重要的定量实验。请回答下列问题:
I.某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol·L-1盐酸、0.55mol·L-1 NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
| 实 验 试剂如下 |
溶 液 温 度 |
中和热 △H |
||||
| t1 |
t2 |
|||||
| ① |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.3℃ |
||
| ② |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.5℃ |
||
已知:Q(放)="C" m(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1·Kg-1,m指溶液的质量,各物质的密度均为1g·cm-3。
①计算分析△H= 。(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
II.为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0 g试样,加水溶解,配成250 mL试样溶液。
②用酸式滴定管量取25.00 mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500 mol/L NaOH溶液滴定,消耗NaOH溶液20.00 mL。
③再取25.00 mL试样溶液放入另一锥形瓶中,用0.1000 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00 mL。
回答下列问题:
(1)已知:0.10 mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为
(2) 完成并配平下列离子方程式
C2O42- + MnO4- + H+ = CO2 + Mn2+ +
(3) 步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4·2H2O的质量分数 。(填“偏大”、“偏小”或“无影响”)
(4) 步骤③中判断滴定终点的方法是 。
(5)常温下0.01 mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示
①写出H2C2O4的电离方程式_________ __________________。
②KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题) _______________
③向0.1 mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是______。
A.c K+) = c(HC2O4-) + c(H2C2O4) + c(C2O42-)
B.c(Na+) = c(H2C2O4) + c(C2O42-)
C.c(K+) + c(Na+) = c(HC2O4-) + c(C2O42-)
D.c(K+) > c(Na+)
实验室欲配制0.5mol·L-1的NaOH溶液500mL,有以下仪器:①烧杯② 100mL量筒 ③100mL容量瓶④胶头滴管⑤玻璃棒⑥托盘天平(带砝码)⑦药匙
(1)配制时,必须使用的仪器有____________(填代号),还缺少的仪器是___________。该实验中两次用到玻璃棒,其作用分别是_________________,__________________。
(2)配制溶液时,一般可以分为以下几个步骤: ①称量②计算 ③溶解 ④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却,其正确的操作顺序为__________________________(用序号填空),其中在①操作中需称量NaOH______________g。
(3)下列操作结果会使溶液的物质的量浓度偏低的是_________ 。
| A.没有将洗涤液转入容量瓶中 |
| B.称量时用了生锈的砝码 |
| C.定容时,俯视容量瓶的刻度线 |
| D.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度 |
(4)若某学生用托盘天平称量药品时,在托盘天平左盘放有20g砝码,天平达平衡时游码的位置如图,则该同学所称量药品的实际质量为_________g。
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图I~IV所示。
(1)只根据图I、II所示实验,能够达到实验目的的是(填装置序号)__________。
(2)图III、IV所示实验均能鉴别这两种物质,其反应的化学方程式为___________________;与实验III相比,实验IV的优点是(填选项序号)__________。
| A.III比IV复杂 |
| B.IV比III安全 |
| C.IV比III操作简便 |
| D.IV可以做到用一套装置同时进行两个对比实验,而III不行 |
(3)若用实验V验证酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式)______。
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。
①当石灰水过量时,其离子方程式为___________;②碳酸氢钠与氢氧化钙的物质的量之比是2:1时,所得溶液中的溶质的化学式为______。
为了确认电解质溶液X的成分,某同学做了以下两组实验,请根据实验回答问题:
| 编号 |
I |
II |
| 实验一 |
  |
 |
| 编号 |
III |
|
| 实验二 |
 |
(一)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合: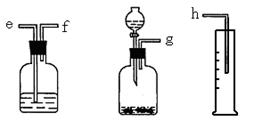
(1)标出各仪器连接的顺序 ,量筒在实验中的作用是
(2)有一块表面氧化成Na2O的金属钠,其质量为1.0g,实验后在量筒中收集到0.224L水,求样品中金属钠的质量是 。(假设在标准状况下测定)
(二)为探究碳酸氢钠的热稳定性,并验证其产物与过氧化钠的反应,按以下装置图进行实验,填写有关现象及化学方程式。
(1)写出A中发生反应的化学方程式为____________________
(2)B中浓硫酸的作用是____________________
(3)C中发生反应的化学方程式为___________________,每反应1molNa2O2转移________mol电子
(4)E中收集的气体是__________________