某化学小组按下图所示实验流程比较浓硝酸和稀硝酸的氧化性强弱,其中B为一种紫红色金属,C为红棕色气体。
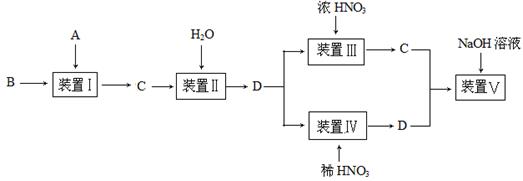
请回答下列问题:
(1)A与B反应的化学方程式是 ;A与B反应迅速,实验中需要采取措施控制气体放出的快慢,则装置Ⅰ所选择的主要仪器为 (不包括铁架台、铁夹、橡皮塞和导管等)。
(2)实验时在装置Ⅰ中加入B后,在加入A之前需向整套装置中通入足量的CO2气体,该操作的目的是 。实验室制取CO2气体的化学方程式是 。
(3)装置Ⅱ中发生反应的化学方程式是 。
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸 (填“强”或“弱”),判断的依据 是 。
(5)小组内有同学指出该流程中装置Ⅴ可有可无,你认为装置Ⅴ是否需要 (填“是”或“否”),理由是 。
工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁(已知炽热铁屑与氯化氢生成氯化亚铁)。现用如图所示的装置模拟上述过程进行试验。
回答下列问题:
(1)盛装浓盐酸的仪器名称为 ,进行实验时,应先点燃 (选填A或C)处酒精灯。
(2)制取无水氯化铁的实验中,A中反应的离子方程式为 ,装置B中加入的试剂是 。
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是 (化学方程式表示)。为除去氯气中混有的少量HCl,可以在装置A、B间加入装有 的洗气瓶。
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____________(填化学式)。长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____________(填数字代号)。
① O2 ② Cl2 ③ CO2 ④ HClO
测定硫酸铜晶体(CuSO4·xH2O)中x值的实验过程如下。完成下列填空:
(1)设待测硫酸铜晶体的化学式为CuSO4·xH2O ,则该硫酸铜晶体受热失去全部结晶水的化学方程式为 。
(2)下列是实验中用到的几种仪器,仪器与对应名称正确的是 。(填序号)
(3)“冷却”操作应在 (填仪器名称)中进行,“灼烧”时热源选用的是酒精灯而不是酒精喷灯,理由是 。
(4)恒重操作的目的是 。
(5)测定硫酸铜晶体结晶水含量时,若实验结果偏低,原因可能是 。(填序号)
a.坩埚未完全干燥b.加热过程中晶体有少量溅失
c.坩埚上沾有受热不分解的杂质 d.加热后未放入干燥器中冷却
(6)下面是某学生实验的一次数据,请完成计算
| 加热前质量 |
加热后质量 |
||
| m1 |
m2 |
m3 |
m4 |
| 11.721g |
22.692g |
18.631g |
a |
①若无需再进行第三次称量,则a的数值范围应为 。
②若加热后坩埚与固体总质量为18.631g,实测值x= (保留两位小数)
③若理论值x=5,则该实验的相对误差是 。
实验题组
Ⅰ.下图所示的实验,能达到实验目的的是 。
| A |
B |
C |
D |
 |
 |
 |
 |
| 验证化学能 转化为电能 |
验证温度对化学平衡的影响 |
验证铁 发生析氢腐蚀 |
验证AgCl 溶解度大于Ag2S |
Ⅱ.某同学为了验证Fe3+是否能氧化H2SO3生成了SO42–,他用50mL0.1mol/LFeCl3溶液吸收制取SO2气体的尾气,再进行以下实验:
(1)向FeCl3溶液中通入一定量的SO2,反应的离子方程式: ;
(2)检验吸收液中SO42–的方法: ;
(3)吸收液中除了含有H+、Cl–、SO42–以外,对其它成份(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。
假设1:溶液中存在Fe3+、Fe2+;
假设2:溶液中存在 ;
假设3:溶液中存在Fe2+ 而不存在H2SO3(二者恰好完全反应)。
②设计方案、进行实验,验证假设。请在表中写出实验步骤以及预期现象和结论(可以不填满)。限选实验试剂和仪器:试管、滴管、0.1moL L-1KMnO4、0.1moL
L-1KMnO4、0.1moL L-1KSCN溶液、品红溶液。
L-1KSCN溶液、品红溶液。
| 实验步骤 |
预期现象和结论 |
| 步骤1:用试管取样品溶液2~3mL,再用滴管取 |
(1) 若出现红色,则假设1成立; (2)若未出现红色,则假设2或假设3成立。 |
步骤2: |
|
己二酸 是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酷化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酷化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:

可能用到的有关数据如下:
| 物质 |
密度(g/cm3) |
熔点 |
沸点 |
溶解性 |
相对分子质量 |
| 环己醇 |
0.962g/cm3 |
25.9℃ |
160.8℃ |
20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
100 |
| 己二酸 |
1.360g/cm3 |
152℃ |
337.5℃ |
在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
146 |
实验步骤如下:
Ⅰ、在三口烧瓶中加入16mL 50%的硝酸(密度为l.3lg/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇。
Ⅱ、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ、当环己醇全部加入后,将混合物用80℃-90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
Ⅴ、粗产品经提纯后称重为5.7g。
请回答下列问题:
(1)滴液漏斗的细支管a的作用是________,仪器b的名称为________。
(2)己知用NaOH溶液吸收尾气时发生的相关反应方程式为:2NO2+2NaOH=NaNO2+NaNO3+H2O NO+NO2+2NaOH =2NaNO2+H2O;如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为:________、________
(3)向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则可能造成较严重的后果,试列举一条可能产生的后果:__________,
(4)为了除去可能的杂质和减少产品损失,可分别用冰水和________洗涤晶体。
(5)粗产品可用________法提纯(填实验操作名称)。本实验所得到的己二酸产率为________。
草酸亚铁为黄色固体,作为一种化工原料, 可广泛用于涂料、染料、陶瓷、玻璃器皿等的着色剂以及新型电池材料、感光材料的生产。合成草酸亚铁的流程如下:
(1)配制(NH4)2Fe(SO4)2溶液时,需加入少量稀硫酸,目的是 。
(2)得到的草酸亚铁沉淀需充分洗涤,检验是否洗涤干净的方法是 。
(3)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行加热分解,结果如下图(TG%表示残留固体质量占原样品总质量的百分数)。
①则A→B发生反应的化学方程式为: 。
②已知B→C过程中有等物质的量的两种气态氧化物生成,写出B→C的化学方程式 ;
(4)某草酸亚铁样品中含有少量草酸铵。为了测定不纯产品中草酸根的含量,某同学做了如下分析实验:
Ⅰ.准确称量m g样品,溶于少量2mol/L硫酸中并用100mL容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高锰酸钾标准溶液滴定,溶液变为淡紫色,消耗高锰酸钾溶液的体积为V1 mL。
Ⅲ.向上述溶液中加入足量Zn粉,使溶液中的Fe3+恰好全部还原为Fe2+。
Ⅳ.过滤,洗涤剩余的锌粉和锥形瓶,洗涤液并入滤液
Ⅴ.用c mol/L KMnO4溶液滴定该滤液至溶液出现淡紫色,消耗KMnO4溶液的体积V2 mL。
已知:2MnO4-+5H2C2O4+6H+=2Mn2+ +10CO2+8H2O
MnO4-+8H++5Fe2+=5Fe3+ + Mn2++4H2O
回答下列问题:
①若省略步骤Ⅳ,则测定的草酸根离子含量 (填“偏大”、“偏小”或“不变”)。
②m g样品中草酸根离子的物质的量为 (用c,V1,V2的式子表示,不必化简)。