金属镁有许多重要的用途,法国化学家维多克·格利雅因发明了在有机合成方面用途广泛的格利雅试剂而荣获诺贝尔化学奖,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图: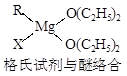
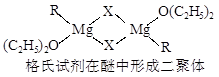
①标出格氏试剂 中的配位键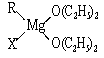
②下列比较中正确的是
A.金属键的强弱:Mg>Al B.基态原子第一电离能:Mg>Al
C.金属性:Mg>Al D.晶格能:KCl>NaCl
E.电负性:Mg>Al F.硬度:Mg>Al 
③二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
A.苯与B3N3H6互为等电子体
www.kB.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
A是化学实验室中常见的有机物,它易溶于水并有特殊香味,B的产量可衡量一个国家石油化工发展的水平,并能进行如图所示的多种反应.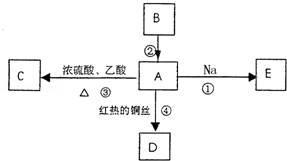
(1)写出A的化学式
(2)写出下列反应的化学方程式
反应①:
反应③:
反应④:
(3)比较反应①与钠和水反应的现象有什么相同和不同
相同点:
不同点:
(1)如图,若烧瓶是干燥的.
当烧瓶口向上时,由A口导入气体,可收集下列中的(填序号,下同)气体.若烧瓶充满水,可收集下列中的气体.①NO ②NH3 ③SO2 ④NO2
(2)若烧瓶中事先已集满一瓶氨气,并将烧瓶口向下放置,由口导入气体可收集NO气体,其原因是.
A、B、C、D四种短周期元素,原子序数D>C>B>A,且B、C、D同周期,A、D同主族,B原子的最外层只有一个电子,C的原子结构示意图为 ,D在同周期元素中原子半径最小,据此填空:
,D在同周期元素中原子半径最小,据此填空:
(1)C元素的名称为,其气态氢化物的化学式为.
(2)D在周期表的周期,族.
(3)A、B、C、D四种元素的原子半径由大到小的顺序为(用化学式填写).
(4)B的最高价氧化物的水化物的化学式为.
无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、
Fe2O3)为原料制备无水AlCl3的工艺流程如下。
(1)氯化炉中Al2O3、Cl2和C反应的化学方程式为________________。
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式为_____________。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是________________。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液中,滤出沉淀物,经洗涤、灼烧、冷却、称重,得其质量为0.32 g。
①写出上述除杂过程中涉及的离子方程式____________________________。
②AlCl3产品的纯度为________。
(5)工业上另一种以铝灰为原料制备无水AlCl3的工艺中,最后一步是由AlCl3·6H2O脱水制备无水AlCl3,实现这一步的方法是_______________________________________。
(10分)Na+浓度为0.5 mol·L-1的某澄清溶液中,还可能含有下表中的若干种离子。
| 阳离子 |
K+Ag+Mg2+Ba2+ |
| 阴离子 |
NO CO CO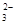 SiO SiO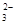 SO SO |
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
| 序号 |
实验内容 |
实验结果 |
| Ⅰ |
向该溶液中加入足量稀盐酸 |
产生白色沉淀并放出标准状况下0.56 L气体 |
| Ⅱ |
将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 |
固体质量为2.4 g |
| Ⅲ |
向Ⅱ的滤液中滴加BaCl2溶液 |
无明显现象 |
请回答下列问题。
(1)实验Ⅰ能确定一定不存在的离子是________。
(2)实验Ⅰ中生成沉淀的离子方程式为___________________________。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?)。
| 阴离子 |
NO |
CO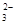 |
SiO |
SO |
| c/(mol·L-1) |
(4)判断K+是否存在,若存在,求出其最小浓度,若不存在说明理由:____________________