㈠如图是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元)。晶体中氧的化合价可看作是部分为0价,部分为-2价。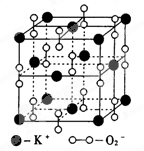
⑴该结构与 的结构相似(填选项字母,下同)
A.NaCl B.CsCl C.干冰 D.SiO2
⑵钾、氧两元素所形成化合物的化学式是
A.K2O B.K2O2 C.K2O3 D.KO2
⑶下列对KO2晶体结构的描述正确的是
A.晶体中与每个K+距离最近的K+有8个
B.晶体中每个K+周围有8个O2-,每个O2-周围有8个K+
C.每个 O2-周围最近且等距离的K+所围成的空间构型为正八面体
D.晶体中,0价氧原子与-2价氧原子的数目比为3: 1
㈡如右图所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解池,其电极材料见右图: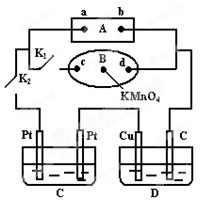
⑴关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向c端移动,则电源b端为 极,通电一段时间后,观察到滤纸d端的电极反应式是 ;
⑵已知C装置中溶液为Cu(NO3)2和Y(NO3)3,且均为0.1mol,打开K1,关闭K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如右图所示。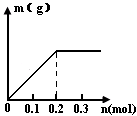
则Cu2+、Y3+、H+氧化能力由大到小的顺序是 ;D装置中溶液是H2SO4,则电极C端的实验现象是_____ 。
(共12分)物质之间的转化关系如下图,其中A、D、E、F、H为常见单质,其余为化合物,且单质E和单质F在点燃或加热的条件下生成淡黄色的固体,B常温下为液态化合物。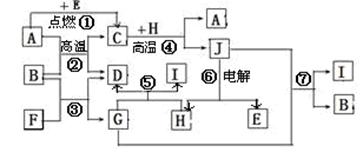
试回答下列有关问题:
(1)A在元素周期表的位置周期族。
(2)分别写出反应②⑦的化学方程式;。
(3)写出引发反应④的实验操作;
(4)写出用A与H作电极材料插入G溶液形成闭合电路后的负极反应式是:
。
(5)写出上图中物质C与稀HNO3溶液反应的离子方程式:。
(9分)有一包白色粉末状混合物,可能含有Na2CO3、NaCl、CaCO3、CuSO4、KCl、Na2SO4、MgCl2、KNO3中的某几种,现进行如下实验:
①将混合物溶于水,得到无色透明溶液。
②取少量上述溶液两份,其中一份加入BaCl2溶液,立即产生白色沉淀,再加上稀硝酸,沉淀不溶解,在另一份中加入NaOH溶液,也产生白色沉淀。
根据上述实验现象回答:
(1)原混合物中肯定没有__________________________。
(2)原混合物中肯定有____________________________。
(3)不能确定是否含有____________________________。
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示: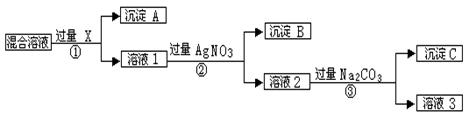
请回答下列问题:
⑴写出实验流程中下列物质的化学式
试剂X :沉淀A:沉淀B:
⑵上述实验流程中加入过量的Na2CO3的目的是。
⑶按此实验方案得到的溶液3中肯定含有(填化学式)杂质。
丁基橡胶可用于制造汽车内胎,合成丁基橡胶的一种单体A的分子式为C4H8,A氢化后得到2—甲基丙烷。完成下列填空:
1)A可以聚合,写出A的两种聚合产物________________、
2)A与某烷发生烷基化反应生成分子式为C8H18的物质B,B的一卤代物只有4种,且碳链不对称。写出B的结构简式_________________。
3)写出将A通入下列两种溶液后出现的现象。
A通入溴水:____________________________
A通入溴的四氯化碳溶液:_________________________
4)烯烃和NBS作用,烯烃中与双键碳相邻碳原子上的一个氢原子被溴原子取代。分子式为C4H8的烃和NBS作用,得到的一溴代烯烃有3种,分别写出其结构简式_______
用石油裂化和裂解过程得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下:
根据以上材料和你所学的化学知识回答下列问题:
(1)由CH2=CH2制得有机物A的化学方程式:,反应类型是。
(2)A与B合成丙烯酸乙酯的化学反应方程式是:。该反应的类型是。
(3)由石油裂解产物乙烯合成聚乙烯塑料的化学方程式是:。