某研究性学习小组用FeCl3溶液做“腐蚀液”,制作印刷电路板,其反应原理是:2FeCl3+Cu=2FeCl2+CuCl2。
【实验探究】
(1)通过《化学1》的学习,知道了有离子参加的化学反应为离子反应。离子反应可用离子方程式表示。请写出2FeCl3+Cu=2FeCl2+CuCl2反应的离子方程式为: 。
(2)若要溶解电路板上3.2g的铜,则至少需要FeCl3物质的量为 mol。
(3)使用后失效的“腐蚀液”为废液,验证废液中是否存在Fe3+的试剂是 ,加入该试剂后,若出现 现象,说明废液中还存在Fe3+。
(4)废液中的CuCl2可通过加入足量的 ,反应后转化成铜且能使所得溶液中含有单一溶质。
(5)回收Cu后的废液,通入足量的Cl2,可以重新获得FeCl3溶液,其反应的化学方程式为 。
【实验结论】
利用FeCl3溶液做印刷电路板的“腐蚀液”,不仅废液中的铜可以得到回收,经过处理后的废液还可以重新使用。
【知识拓展】
(6)铁元素是维持生命活动不可缺少的微量元素,虽然人体中通常只含有3~5g铁元素,但铁元素在人体中却发挥着重要作用,人体缺铁会引起 疾病。
(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图甲所示。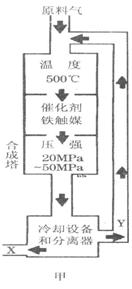

①X的化学式为__________,属于________(填“极性”或“非极性”)分子。 ②图甲中条件选定的主要原因是(选填字母序号,下同)________。
②图甲中条件选定的主要原因是(选填字母序号,下同)________。
A.温度、压强对化学平衡的影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动。图乙表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是________,当横坐标为温度时,变化趋势正确的是__________。
(2)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水的过程中存在的可逆反应:
___________________________________________________________________。
②氨水中水电离出的c(H+)___________10-7 mol/L(填“>”、“<”或“=”)。
③将氨水和盐酸混合后, 某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-)D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
Ⅰ、若溶液中只溶解了一种溶质,该溶质的名称是,上述离子浓度大小顺序关系中正确的是(选填序号)。
Ⅱ、若上述关系中C是正确的,则溶液中溶质的化学式是。
Ⅲ、若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前
c(HCl)c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)c(Cl-)。
(3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成X和Y两种物质。X为铵盐,Y在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96 L氨气(标准状况),同时生成0.3 mol X。
①写出氨气和氟气反应的化学方程式: ___________________________________。
②在标准状况下,每生成1 mol Y,转移电子的物质的量为___________mol。
(4)已知液态NH3与H2O相似,也可以发生微弱的电离,电离出含有相同电子数的微粒,则液态NH3的电离方程式为:
镁在空气中燃烧除生成MgO外,还可能生成Mg3N2。某校化学兴趣小组的同学利用镁在空气中燃烧后的固体(不含单质)进行实验,探究其组成。
(1)甲组同学取一定量燃烧后的固体投入水中,得到了一种能使湿润的红色石蕊试纸变蓝 的气体,该气体的化学式为,说明固体中含有Mg3N2,生成该气体的化学反应方程式为。
(2)乙组同学为测定Mg3N2含量,用图示装置进行实验,充分反应后再加热A。其中浓硫酸的作用是,对A加热的目的是 。已知加入的固体质量为4.0g,最终C装置增重ag,则固体中含Mg3N2g(用含a的式子表示)。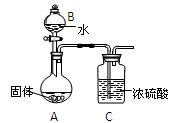
(3)丙组有的同学认为乙组同学的测定结果偏高,理由是
。
有的同学认为乙组同学的测定结果偏低,理由是
。
丙组同学进行了改进,他们将乙组同学实验中得到的难溶固体进行过滤、洗涤、干燥,并
灼烧固体至恒重,测得其质量为4.08g。上述过程中,洗涤沉淀的操作是
。
镁在空气中燃烧后生成的固体中Mg3N2的质量分数为。
(4)有一种用铵盐与含镁矿石混合煅烧制取氧化镁的方法,解决了现有方法存在的原料成 本高、项目投资大、能耗高、副产品不好用等问题,其原理是将含镁矿石粉(含氧化镁)与 铵盐混合,经过煅烧、水溶、过滤,得到粗镁盐溶液,并回收煅烧产生的氨。写出用固体(NH4)2SO4与含镁矿石粉煅烧的化学反应方程式
。
有机化合物A的相对分子质量为153,A有如下的性质:
Ⅰ.取A的溶液少许,加入NaHCO3溶液,有气体放出。
Ⅱ.另取A的溶液,向其中加入足量的NaOH溶液,加热反应一段时间后,再加入过量的
HNO3酸化的AgNO3溶液,有淡黄色沉淀生成。
A有如下的转化: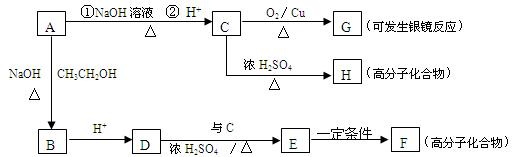
请填空:
(1)A物质的结构简式。
(2)C→G的反应类型;A→B的反应类型。
(3)写出与C具有相同官能团的同分异构体的结构简式;
G与过量的银氨溶液反应,每生成2.16克Ag,消耗G的物质的量是mol。
(4)写出下列反应的化学方程式:
D→E。
C→H。
一无色气体,可能由CO2、HCl、NH3、NO2、NO、H2中的一种或几种组成。将此无色气体通过盛有浓H2SO4的洗气瓶,发现气体体积减少。继续通过装有固体Na2O2的干燥管,发现从出气管出来的气体颜色显红棕色,再将该气体全部通入盛满水倒立于水槽中的试管内,发现最后试管里仍然为一满试管液体。由此可推知:①原气体中一定含有_____________,一定不会有____________;②最终结果可知原气体中______与_______气体的体积比为_______。
某学生设计氨催化氧化实验,并将制得的NO进一步氧化为NO2,用水吸收NO2,并检验HNO3的生成。可供选择的固体药品有:NH4Cl、Ca(OH)2、KClO3、MnO2、CaO。可供选择的液体药品有:H2O2、浓盐酸、水。可供选择的仪器有: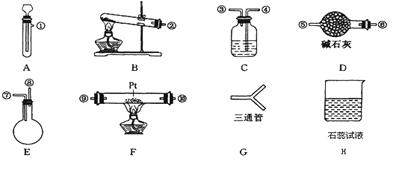
另有铁架台、铁夹、铁圈、乳胶管若干,可供选择。设计实验时,A和B两个制气装置均允许使用两次,其余装置只能使用一次。
(1)氨氧化制NO的化学反应应在装置中进行。
(2)制取NH3的装置最好选择,其化学反应方程式为;为快速制取O2的装置最好选择,其化学反应方程式为。
(3)各仪器按气流方向连接的正确顺序为:
A、B→G→→ F →→→ H。(按装置先后排列顺序补充完整)
(4)装置C的作用是。
( 5 ) 如果实验前需收集一试管的氨气,如何采用一种简易方法检验试管中
氨气是否集满(简述操作、现象和结论)?
(6)装置H中溶液显红色,其原因是
(7)请据以上实验事实设计一个实验来检验一份白色药品是铵盐,写出其正确
的实验操作步骤