某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
| 时间/s |
0 |
5 |
10 |
15 |
| 读数/g |
215.2 |
211.4 |
208.6 |
208.6 |
请你据此分析计算:
(1)实验中产生的CO2气体质量为 ;
(2)该产品中碳酸钠的质量分数 (结果精确到小数点后一位) 。
A是一种含碳、氢、氧三种元素的有机化合物,已知:A相对分子质量为144,其中碳的质量分数为50%。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B和甲醇。B中碳、氢、氧原子个数比为1:1:1,分子中没有支链,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有(选填编号)
①加成反应②酯化反应③加聚反应④氧化反应
(2)B分子所含官能团的名称是、。
(3)与B具有相同官能团的同分异构体的结构简式是 ________________________________________________。
(4)由B制取A的化学方程式是:。
(8分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:
这种材料可采用如下图所示的合成路线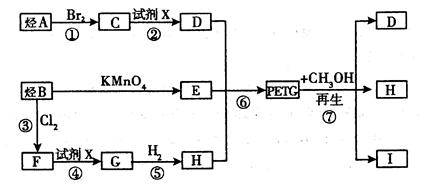
(1) 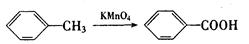
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1)⑦的反应类型是 。
(2)写出I的结构简式: 。
(3)合成时应控制的单体的物质的量:n(H):n(E):n (D)=(用m、n表示)。
(4)写出反应②的化学方程式:
(5)写出同时符合下列两项要求的E的所有同分异构体的结构简式。
①该同分异构体的苯环上相邻的三个碳原子上都连有取代基。
②该同分异构体在一定条件下能发生银镜反应和水解反应,遇到FeCl3溶液显紫色。
、 、 。
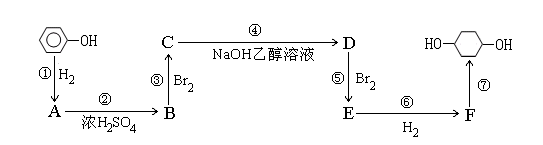
以苯酚为原料的合成路线如下所示,请按要求作答:
(1)写出以下物质的结构简式:BF
(2)写出反应①④的化学反应方程式:
①
④
(3)反应⑤可以得到E,同时可能得到的副产物的结构简式为:
书写下列反应的化学方程式:
(1)、丙烯加聚
(2)、乙醛的银镜反应
(3)、2-丙醇的催化氧化
(4)、由甲苯制TNT炸药
(5)、实验室制取乙炔
室安卡因(G)是一种抗心率天常药物,可由下列路线合成;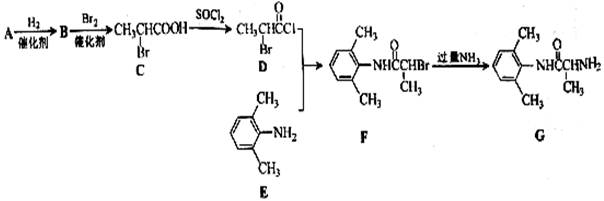
(1)已知A是 的单体,则A中含有的官能团是(写名称)。B的结构简式是。
的单体,则A中含有的官能团是(写名称)。B的结构简式是。
(2)C的名称(系统命名)是,C与足量NaOH醇溶液共热时反应的化学方程式是。
(3)X是E的同分异构体,X分子中含有苯环,且苯环上一氯代物只有两种,则X所有可能的结构简式有 、、、。
、、、。
(4)F→G的反应类型是。
(5)下列关于室安卡因(G)的说法正确的是。
a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色
c.能与盐酸反应生成盐 d..属于氨基酸