小华同学用下图所示的装置进行中和反应实验,反应后为确定盐酸和氢氧化钠是否恰好完全中和,他取出少量反应后的溶液于试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论。
⑴请写出发生的反应方程式 ;
⑵小亮认为小华的结论不正确,他认为除了“恰好中和”外还有第二种可能性,这种可能性是 ;
⑶请你另外设计一个实验,探究上述烧杯中的溶液是否恰好完全中和。
| 实验 |
实验操作 |
实验现象 |
实验结论 |
| 甲 |
取样于试管中,加入几滴紫色石蕊溶液 |
|
恰好中和 |
| 乙 |
取样于试管中,加入 |
产生气泡 |
第二种可能性 |
某同学将光亮的镁条放入滴有酚酞的NaHCO3饱和溶液中,产生大量气泡和白色固体,溶液红色加深。
一、溶液红色加深,则反应后溶液的碱性(填“增强”、“不变”或“减弱”)。
二、为确定气体和固体的成分,该同学进行了如下的探究。
(1)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象。则该气体为(写化学式)。
(2)对白色固体做出如下猜测并进行实验:
【猜测】
查阅资料1:Mg(HCO3)2能溶于水。
①白色固体可能是MgCO3;
② 白色固体可能是;
③白色固体可能是MgCO3和Mg(OH)2。
【实验】
① 取洗净后的白色固体,加入足量的溶液,观察到,则白色固体一定含有MgCO3。
查阅资料2:MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
②为进一步确定白色固体的组成,该同学进行了定量实验:
称取干燥的白色固体22.6 g,充分加热至不再产生气体为止,并使分解产生的气体全部先通过浓硫酸,浓硫酸增重1.8g,则白色固体中含有,再通过碱石灰,碱石灰增重8.8g,则固体中MgCO3与Mg(OH)2的质量比为。
有一包固体样品,可能是碳酸钠、硫酸铜、氢氧化钠、氯化钡中的一种或几种。为探究其成分,李老师取用一定量样品,加水溶解,过滤得到白色沉淀甲和无色滤液乙。
【探究活动一】自主小组探究白色沉淀甲的成分。
| 实验操作 |
实验现象 |
结论 |
| 取白色沉淀甲,滴加足量的稀盐酸 |
沉淀消失 |
白色沉淀甲中一定含有 |
【探究活动二】合作小组探究固体样品中是否含有氢氧化钠,设计了如下实验:
| 实验步骤 |
实验操作 |
实验现象 |
结论 |
| 1 |
取无色滤液乙,加入碳酸钠溶液 |
无明显现象 |
无色滤液乙中一定不含氯化钡 |
| 2 |
取适量无色滤液乙,加入过量的溶液,过滤 |
生成白色沉淀 |
无色溶液中一定含有碳酸钠 |
| 3 |
取实验步骤2中的滤液,滴加溶液 |
原固体样品中一定存在氢氧化钠 |
【反思】实验步骤2中加入过量试剂的目的是。
【结论】通过两个小组的共同探究,得出了原固体样品中含有的成分。
实验室按如图所示的装置制取二氧化碳气体,并探究二氧化碳的性质,试回答以下问题:
(1)用装置A来制取CO2所用的药品是、(写名称);
(2)若要用装置B鉴定CO2,在B中应盛放的试剂名称是;
(3)当将标①②的导管连接时,B中看到的实验现象是;
(4)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是;
(5)当将标①和③的导管连接时,C中看到的实验现象是,烧杯D中放有燃着的蜡烛,当将标有①和④的导管连接时,D中看到的实验现象是,证明CO2有、的性质。
某兴趣小组的同学为了探究一久置氢氧化钠溶液是否变质,进行了如下猜想与实验:
【查阅资料】氯化钡溶液显中性,碳酸钠溶液显碱性
【提出猜想】假设一:该溶液没有变质;
假设二:该溶液部分变质;
假设三:该溶液变质
【实验验证】
| 实验探究 |
实验现象 |
实验结论 |
| ①取少量该溶液于试管中,向其中滴加过量的氯化钡溶液 |
生成白色沉淀 |
假设不成立 |
| ②静置,向上层清液中滴加酚酞溶液 |
溶液 |
假设二成立 |
【讨论交流】
(1)步骤①滴加过量的氯化钡溶液的目的是.
(2)某同学设计了如下方案:①取少量样品溶液向其中滴加少量氯化钡溶液产生白色沉淀;②另取少量样品溶液再向其中滴加酚酞溶液,观察到溶液呈红色。由此他得出了假设二成立的结论。
他的结论(填“正确”或“不正确”)理由是。
(3)久置氢氧化钠敞口放置变质的原因是(用化学方程式表示),因此氢氧化钠应保存。
某化学课外活动小组在实验室配制石灰水时,因发现烧杯底部有固体未溶解,对熟石灰样品的主要成分进行了探究.请你参与讨论并完成实验报告.
【提出问题】针对该熟石灰样品的成分,同学们展开了讨论,小明认为溶解后剩余固体为变质后的难溶性物质,变质的化学方程式为 。小华同学不同意他的判断,你认为小华同学的理由是。
【进行猜想】猜想一:熟石灰样品成分是Ca(OH)2;
猜想二:熟石灰样品成分是CaCO3;
猜想三:你认为熟石灰样品成分还可能是。
【实验与结论】请你通过实验验证你的猜想:
【拓展与应用】实验小组同学想测定样品中Ca(OH)2的质量分数:称取上述0.5g样品,加足量水使之充分溶解,搅拌后过滤.
①甲组在实验室用pH试纸和配制好的10%盐酸溶液进行实验,实验数据记录见下表.(提示:氯化钙溶液呈中性)
| 加入盐酸溶液的质量/g |
0 |
2.5 |
3.65 |
6 |
| 样品的pH |
12 |
11 |
7 |
2 |
I.边滴加稀盐酸,边不断搅拌的目的是 ;
II.样品中Ca(OH)2的质量分数是多少?(写出计算过程,4分)
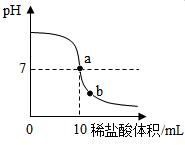
②乙组同学进行了数字化实验,由计算机描绘出了整个实验过程中溶液pH的变化图象如下图.则图中a点表示的含义是;
图中b点溶液中含有的溶质有(填化学式),乙组同学要计算出样品中氢氧化钙的质量分数,除了要用到已有数据外,你认为还需要的数据是。