(1) 、—CH3、
、—CH3、 都是重要的有机反应中间体,有关它们的说法正确的是_________________
都是重要的有机反应中间体,有关它们的说法正确的是_________________
| A.它们均由甲烷去掉一个氢原子所得 |
| B.它们互为等电子体,碳原子均采取sp2杂化 |
| C.CH与NH3、H3O+互为等电子体,几何构型均为三角锥形 |
D. 中的碳原子采取sp2杂化,所有原子均共面 中的碳原子采取sp2杂化,所有原子均共面 |
E.两个—CH3或一个 和一个
和一个 结合均可得到CH3CH3
结合均可得到CH3CH3
(2)锌是一种重要的金属,锌及其化合物有着广泛的应用。
①指出锌在周期表中的位置:第________周期,第________族,属于________区。
②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。葡萄糖分子中碳原子杂化方式有___________;写出基态Zn原子的电子排布式___________________。
在第3周期中,化学性质最稳定的元素符号是,最高价氧化物的水化物的酸性最强的化合物的化学式是,碱性最强的化合物的化学式是,显两性的氢氧化物的化学式是,该两性氢氧化物与氢氧化钠溶液反应的离子方程式为。
双安妥明是一种降血脂药物,主要用于降低血液中胆固醇浓度,安全,副作用小,其结构简式为

已知:C的分子式为C4H8,且支链有二个甲基;I能发生银镜反应且1mol I能与2mol H2发生加成反应;K的结构具有对称性。试回答下列问题:
(1)双安妥明的分子式为: 。
。
(2)C的结构简式为:___ 。
。
(3)反应②的条件是____。
(4)J写银氨溶液发生反应的离子方程式为:。
(5)反应④的化学方程式为:_____。
(6)符合下列3个条件的H的同分异构体有____种,其中在核磁共振氢谱中出现五组峰的是(写结构筒式)。
①能与FeCl3溶液显色;②苯环上只有2个取代基;③1mol该物质最多可消耗3mol NaOH
X、Y、Z、Q、W为按原予序数由小到大排列的五种短周期元素。已知:①X与Q处于同一主族,其原子价电子排布式都为n s2np2,且X原子半径小于Q;②Y元素是地壳中含量最多的元素;W元素的电负性路小于Y元素,在W原子的价电子排布式中,p轨道上只有1个未成对电子;③Z元素的电离能数据见下表(kJ·mol-1)
s2np2,且X原子半径小于Q;②Y元素是地壳中含量最多的元素;W元素的电负性路小于Y元素,在W原子的价电子排布式中,p轨道上只有1个未成对电子;③Z元素的电离能数据见下表(kJ·mol-1)
| I1 |
I2 |
I3 |
I4 |
… |
| 496 |
4562 |
6912 |
9540 |
… |
请回答:
(1)XY2分子的空间构型为。
(2)QX的晶体结构与金刚石的相似,微粒间存在的作用力是。
(3)晶体ZW的熔点比晶体XW4明显高的原因是。
(4)XY2在高温高压下所形成的晶胞如图所示。该晶体的类型属于(选填“分子”、“原子”、“离子”或“金属”)漏体,该晶体中X原子的杂化形式为___。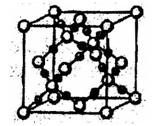
(5)氧化物MO的电子总数与QX的相等,则M为。(填元素符号);MO是优良的耐高温材料,其晶体结构与ZW晶体结构相似,MO的熔点比CaO的高,其原因是。
水是一种重要的自然资源,是人类赖以生存不可缺少的物质,水质优劣直接影响人体健康。请回答下列问题:
(1)某贫困山区,为了寻找合适的饮用水,对山上的泉水进行了分析化验,结果显示水中主要含钙离子、镁离子、氯离子和硫酸根离子。则该硬水属于____(填“暂时”、“永久”)硬度,若要除去Ca2+、Mg2+,可以往水中加入石灰和纯碱,试剂加入时先加______后加___。
(2)我国规定饮用水的硬度不能超过25度。硬度的表示方法是:将水中的Ga2+和Mg2+都看作Ca2+,并将其折算成CaO的质量,通常把l升水中含有10mg CaO称为1度。某化学实验小组对本地区地下水的硬度进行检测,实验过程如下:
实验中涉及的部分反应:M2+(金属离子)+EBT-(铬黑T)= MEBT+
蓝色酒红色
M2+(金属离字)+Y4-(EDTA):MY2-
MEBT++Y4-(EDTA)=MY2-+ EBT-(铬黑T)
①取地下水样品25.00进行预处理。写出由Mg2+引起的暂时硬度的水用加热方法处理时所发生反应的化学方程式。
②预处理的方法是向水样中 加入浓盐酸,煮沸几分钟,煮沸的目的是。
加入浓盐酸,煮沸几分钟,煮沸的目的是。
③将处理后的水样转移到250mL的锥形瓶中,加入氨水一氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.01000·L-1的EDTA标准溶液进行滴定,滴定时眼睛应__ __,滴定终点时的实验现象是
__,滴定终点时的实验现象是 。
。
④滴定终点时共消耗EDTA溶液15.00mL,则该地下水的硬度=。
⑤若实验时装有EDTA标准液的滴定管只用蒸馏水润洗而未用标准液润洗,则测定结果将
(填“偏高”、“偏低”或“无影响”)
某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)已知FeCl3在反应中得到电子,则该反应的还原剂是。
(2)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①电解质溶液X是;
②Cu电极上发生的电极反应式为;
③原电池工作时,盐桥中的离子(填“K+”或“Cl—”)不断进入X溶液中。
(3)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题: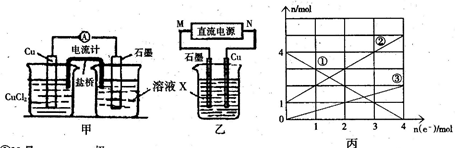
①M是极;
②图丙中的②线是____离子的变化。当电子转移为2mol时,向乙烧杯中加入L 5mol·L-1NaOH溶液才能使所有的金属阳离子沉淀完全。