不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,x越大,其原子吸引电子的能力越强。 下面是某些短周期元素的x值:
| 元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
| x值 |
0.98 |
1.57 |
2.04 |
2.55 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
通过分析x值变化规律,确定Mg的x值范围:_______ < x(Mg) <_________。
推测x值与原子半径的关系是________________________________;根据短周期元素的x值变化特点,体现了元素性质的_________________变化规律。
分别指出下列两种化合物中氧元素的化合价:HClO_________,HFO________。
经验规律告诉我们:当成键的两原子相应元素x数值的差值(Δx),当Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键类型是________________。
预测元素周期表中,x值最小的元素位于______周期________族(放射性元素除外)。
将1molCO和1molH2O充入某固定容积的反应器中,在某条件下达到平衡:
CO+H2O(g)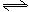 CO2+H2,此时有2/3的CO转化为CO2。
CO2+H2,此时有2/3的CO转化为CO2。
(1)该平衡混合物中CO2的体积分数为
(2)若容器体积为1L,到达平衡所需时间为2分钟,则H2的平均反应速率为
(3)若在相同条件下,向容器中充入1molCO2、1molH2和1molH2O,则达到平衡时与⑴中平衡相比较,平衡应向(填“正反应方向”、“逆反应方向”或“不”)移动,此时平衡混合物中CO2的体积分数可能是下列各值中的
| A.22.2% | B.27.55% | C.33.3% | D.36.8% |
(4)结合(3)中计算结果分析若平衡向正方向移动时,则下列说法中正确的是()
①生成物的产量一定增加;②生成物的体积分数一定增加;
③反应物的转化率一定增大; ④反应物的浓度一定降低;
⑤正反应速率一定大于逆反应速率;⑥一定使用了催化剂.
常温下,将20 g 14%的NaOH溶液跟30 g 24%的NaOH溶液相混合,得到密度为1.25 g/cm3的混合溶液。计算:
(1)该混合溶液中NaOH的质量分数为 。
(2)该混合溶液的物质的量浓度为 。
(3)在1000g水中需加入g NaOH,才能使其浓度恰好与上述混合溶液的浓度相等。
实验室现只有下列几种规格的容量瓶:100mL、200mL、250mL、500mL。某个实验中需要0.50 mol·L-1NaOH溶液450 mL和0.46 mol·L-1硫酸溶液500 mL,根据相关情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),配制上述溶液还需用到的玻璃仪器是 (填仪器名称)。
(2)用18.4 mol/L的浓硫酸配制0.46 mol·L-1硫酸溶液500 mL的实验中, 步用到胶头滴管。
(3)根据计算用托盘天平称取NaOH的质量为 g。若NaOH固体溶解后立即转移至容量瓶,则所得溶液浓度 0.50 mol·L-1(填“大于”、“等于”或“小于”,下同)。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度 0.50 mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为
mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是
。
(1)在标准状况下,有下列物质①4gH2,②33.6LCH4, ③1molH2O,④3.01×1023个O2。其
中含分子数最多的是(填序号,下同) ,质量最大的是 ,体积最小的 ;密度由大到小的顺序为 。
(2)实验室从海藻(含碘元素,以碘离子的形式存在)中提取碘的流程如下:
已知2KI+Cl2=2KCl+I2,步骤④的目的是从含碘的有机溶液中分离出单质碘和回收有机溶液。
I.提取碘的过程中有关的实验操作名称:③ 。
II.有下列实验仪器:A.烧杯 B.玻璃棒 C.表面皿 D.分液漏斗 E.酒精灯
步骤①中必须用到的有(填序号) ,还缺少的玻璃仪器有 。
III.提取碘的过程中,选用的萃取剂可以是 。
A.四氯化碳 B.汽油 C.酒精 D.醋酸
(3)写出实验室制取氯气的化学方程式 。
有以下几种物质:
| A.熔融状态的硝酸钾 | B.硫酸(H2SO4) | C.醋酸(CH3COOH) | D.BaSO4固体 |
E、酒精 F、蔗糖 G、葡萄糖 H、干冰 I、铝 J、碳酸钠固体
K、硫酸钠溶液 L、氢氧化钠固体 M、食盐水 N、石墨
在空格中填写正确的序号。
(1)以上物质中能导电的是 ;
(2)以上物质中属于电解质的是 ;
(3)以上物质中属于非电解质的是 。