小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡。为了解其反应过程,他与学习小组的同学进行了如下探究。
【探究一】小组同学根据所学的化学知识设计并进行了如图所示的实验。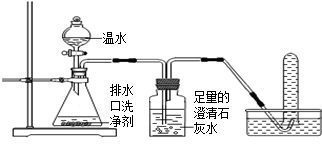
A B C
实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺。由此同学们得出结论:生成的两种气体分别是: (填化学式)。B中有关反应的化学方程式是 。
【探究二】
(1)实验过程:
教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究: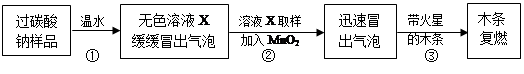
(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设: 根据以上实验现象,X溶液中一定存在的溶质是 ;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种。
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3 + CaCl2 ═ CaCO3↓ + 2NaCl。
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同。
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验。请将下列实验方案填写完整。
| 实验操作 |
主要实验现象 |
结论 |
| ① |
|
证明溶液中有Na2CO3 |
| ② |
|
证明溶液中无NaHCO3 |
| ③ |
|
证明溶液中无NaOH |
(6)实验反思:根据资料,NaHCO3溶液能与石灰水反应生成白色沉淀。于是,同学们猜想:碳酸氢钠与氢氧化钠是否可以发生 (写方程式)这样的反应?于是,同学们进行了新的探究实验。
(10茂名18)以前,人们将石灰石灼烧后的固体与草木灰(主要成分是K2CO3)在水中混合,再取上层澄清液漂洗织物。兴趣小组按上述的操作步骤得到澄清液并对澄清液可能含有哪些物质进行探究。请你利用必需的实验用品和以下限选试剂完成探究过程:
限选试剂:Ba(NO3)2溶液、Na2CO3溶液、NaCl溶液、Ba(OH)2溶液、酚酞试液。
【提出猜想】①含有KOH和Ca(OH)2;②含有KOH、K2CO3和Ca(OH)2;③只含;④含有KOH和K2CO3
【查找资料】K和Na都是活泼金属,它们的化合物化学性质相似;K2CO3溶液显碱性。
【设计与实验】
(1)甲同学要证明猜想①中Ca(OH)2是否存在,选取的试剂是。
(2)请你设计方案,实验验证猜想④,并将相关内容填在下表中(不一定填满,也可以补充)
| 操作步骤 |
预期现象和结论 |
| 步骤1: |
|
| 步骤2: |
【交流讨论】大家认为猜想②肯定不正确,其原因是
。
(10宜昌)26.在高效复习课堂中,同学们利用“硫酸、硝酸钡、氢氧化钠、碳酸钾” 四种物质的溶液对 “复分解反应发生的条件”进行再探究。

【知识回放】
通过判断上述四种溶液两两之间能否发生反应,我能写出其中符合下列条件的两个化学方程式:
⑴一个中和反应;
⑵一个有沉淀生成的反应。
【挖掘实质】
⑴图26-1是HCl和NaOH在水中解离出离子的示意图,小丽发现HCl在水中会 解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推硝酸钡在水中会解离出的离子是(填离子符号)。
解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推硝酸钡在水中会解离出的离子是(填离子符号)。
⑵图26-2是稀盐酸和氢氧化钠溶液发生化学反应的微观过程示意图,该化学反应的实质可以表示为H+ + OH- = H2O
我也能用同样的方式表示上述四种溶液两两之间发生反应时有气体生成的反应的实质。
【实践运用】
⑴通过上述探究发现,在溶液中H+和OH-不能大量共存,我还发现在溶液中和(填离子符号,下同)也不能大量共存。
⑵利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液。经测定,该溶液显酸性。则在该溶液中一定含有的离子是。为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证。
| 溶液中可能含有的离子 |
设计实验验证(实验步骤、现象及对应的结论) |
【知识升华】
对“复分解反应发生的条件”的再探究,我发现在分析多种溶液混合后所得溶液中离子的成分时, 应考虑的因素是。
应考虑的因素是。
(10孝感11)、做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩。小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体。他对此颇感兴趣,决定对其进行探究。
Ⅰ、小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2。
他设法收集气体样品并除去醋酸气体后,用右图实验装置进行探究。将气体依次通过A、B两试剂瓶后,发现A瓶质量增加,B瓶中有白色浑浊物产生。(已知浓硫酸具有吸水性)
实验结论:该气体中一定含有;
Ⅱ、小明对二氧化碳的来源做出了两种猜测:
猜测① 二氧化碳可能是由碳酸氢钠受热分解产生的;
猜测②;
针对以上猜测,小明设计了以下实验:(请你填写下表)
| 实验步骤 |
实验现象 |
实验结论 |
|
| 实验1 |
取碳酸氢钠样品少许加入试管中,加热到不产生气体为止,并把产生的气体通入澄清石灰水 |
试管口有小水滴产生 澄清石灰水变浑浊 |
猜想①正确 |
| 实验2 |
猜想②正确 |
Ⅲ、查阅资料:在百度网页中输入碳酸氢钠的化学性质,可以获知碳酸氢钠受热易分解,产物中有碳酸钠生成。再根据实验Ⅰ写出碳酸氢钠受热分解的化学方程式;
Ⅳ、实验Ⅰ中有白色粉末剩余,请用两种化学方法来验证剩余粉末是碳酸钠(写出实验操作步骤、现象和结论);
方法一:;
方法二:。
(10孝感8)、(5分)氢气具有还原性,能在加热条件下发生反应:H2+CuO Cu+H2O,某同学为了验证氢气还原氧化铜的产物,设计了如下由A、B、C三部分组成的实验装置。
Cu+H2O,某同学为了验证氢气还原氧化铜的产物,设计了如下由A、B、C三部分组成的实验装置。
(1)写出“a”所指仪器名称;
(2)能确认反应生成水的实验现象是;
(3)在实验室里利用A装置还可以制取那些气体?(只要求答一种)
(4)本实验缺少的仪器是;除此之外,上述实验装置还存在不足之处,为了达到实验目的,是根据现象得出的结论更严格更科学,请你提出修改意见。
(10河北35).某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液。实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与。
【提出问题】废液中含有什么物质?
【交流表达】
(1)小明通过观察,认为废液中一定含有硫酸铜。他观察到的现象是。
(2)小红通过分析,认为废液中一定含有硫酸亚铁,她的依据是:
。
【作出猜想】小华认为废液中还可能含有硫酸。
【实验验证】(1)小华测得废液的pH小于7,证明废液中含有硫酸。用pH试纸测定溶液pH的方法:。
(2)小明取少量废液,向其中滴加氢氧化钠溶液,也得到了相同的结论。小明的实验现象是。通过分析与实验,同学们得出废液中含有硫酸亚铁、硫酸铜和硫酸。
【拓展应用】
(1)若将废液中的溶质全部转化为硫酸亚铁,应向废液中加入过量的。写出该反应过程中的一个化学方程式。
(2)反应完全后,过滤,滤渣中物质为,滤液中溶质为硫酸亚铁。