某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是 。
| 第1组 |
第2组 |
第3组 |
| S(单质) |
SO2、X、Na2SO3、NaHSO3 |
SO3、H2SO4、Na2SO4、NaHSO4 |
(2)利用下图所示的装置研究SO2的性质:
(熔点:SO2 -76.1℃,SO3 16.8℃;沸点:SO2 -10℃,SO3 45℃)
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是 。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是 ;装置Ⅲ中溶液逐渐褪色,生成Mn2+,同时pH降低,则该反应的离子方程式是 。
③乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40 mL 2.5mol/L NaOH溶液,反应后增重4.8 g,则装置Ⅳ中发生反应的化学方程式是 。
下图是实验室制取某些常见气体所使用的一些装置和仪器。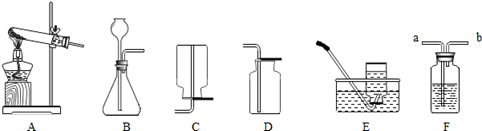
(1)写出实验室制取氧气的一个反应原理 ,用该方法制取氧气的发生装置是 ,收集装置可选择 。
(2)实验室制取二氧化碳,应选择的发生装置是 ,收集装置是 。欲收集满一瓶二氧化碳气体,需要用燃着的小木条放在集气瓶口,若观察到火焰熄灭,则接下来应进行的操作是 。若火焰不熄灭,则说明二氧化碳还没有收集满,应该继续收集。
(3)F装置的用途很广,下列关于该装置的用法正确的是 (将正确答案的序号填在横线上)。
| A.当装置内盛满水,若收集氢气,气体从b通入,若收集氧气,气体从a通入。 |
| B.当装置内盛有一半的浓硫酸时,除去氢气中的水蒸气,气体从b通入 |
| C.当装置内盛满氧气时,将装置内的氧气排除来,水从a通入 |
| D.当装置内盛有一半的水时,观察给病人输氧气的速率,a端连接氧气钢瓶,b端连接病人 |
实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组发现一瓶未密闭的NaOH固体,对其成分提出以下假设,并完成了实验探究。
假设1:只含NaOH;
假设2:含NaOH和Na2CO3;
假设3:只含Na2CO3
(1)成分中可能含有Na2CO3的原因是(用化学方程式回答) 。
(2)取少量样品于试管中,加入足量稀盐酸,观察到________________,说明假设2或假设3成立。
(3)进一步探究的过程如下: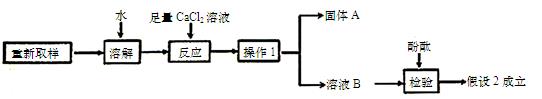
①“操作1”的名称是 ,
②“固体A”的化学式是___________。
③加入足量CaCl2溶液的作用是 。
④溶液B中滴加酚酞后,观察到 ,说明假设2成立。
如图是初中化学中常见的物质之间的转换关系,其中A为常用的食品干燥剂,C为白色沉淀,D为蓝色沉淀,E为红色的固体单质。请你回答问题: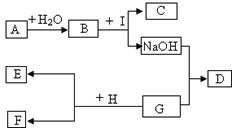
(1)写出物质的化学式:A D
(2)写出反应的化学方程式:
B和I 。基本反应类型是 。
G和H 。基本反应类型是 。
反应现象是 。
(3)这些物质间的反应,没有涉及到的基本反应类型是 。请你用图中的物质写一个符合该基本反应类型的化学方程式 。
现欲探究一固体混合物A的成分,已知其中可能含有BaCl2、Na2CO3、NH4Cl、CuO四种物质中的两种或多种。按图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行)。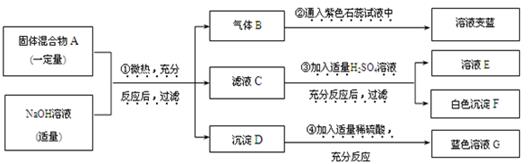
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体 B 的化学式为_______ ____。
(2)滤液 E 中大量存在的阳离子为(写离子符号)_______ ____。
(3)混合物 A 中,肯定不存在的物质是(写化学式)________,理由是_________。
(4)写出实验过程④中发生反应的化学方程式:__________________。
某兴趣小组在实验室发现了一块绿色的孔雀石标本,查阅资料知其主要成分是Cu2(OH)2 CO3。他们以Cu2(OH)2 CO3原料制取铜,其工艺流程如下图所示: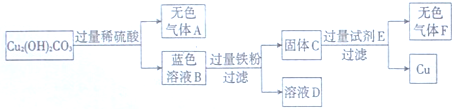
(1)过滤操作中用到的铁制仪器为 。玻璃棒的作用是搅拌和 。
(2)无色气体A的化学式是 ,大气中该气体含量不断上升,会导致 增强,全球气候变暖。
(3)写出蓝色溶液B与铁粉反应的化学方程式 。
(4)试剂E可选用 溶液。写出固体C与试剂E反应的化学方程式 。