小强同学为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。将一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成小球时,撤火,通入氯气,即可见钠着火燃烧。以下叙述错误的是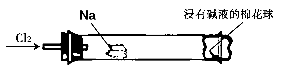
| A.反应生成的大量白色烟雾是氯化钠晶体 |
| B.钠着火燃烧产生苍白色火焰 |
| C.浸有NaOH溶液的棉球用于吸收生成的氯化钠,以免污染空气 |
| D.用湿润的淀粉碘化钾试纸可以检验氯气是否被完全吸收 |
NA为阿伏加德罗常数,下列说法正确的是()
| A.标准状况下,11.2L三氧化硫所含有的原子数目为2NA |
| B.分解H2O2制O2,每生成1 mol O2转移2NA个电子 |
| C.62 g Na2O溶于水后所得溶液中含有O2-数为NA |
| D.常温常压下,1 g H2含有中子数目为NA |
短周期元素X、Y的原子序数相差2。下列有关叙述不正确的是()
| A.X与Y可能位于同一主族 |
| B.X与Y不一定位于同一周期 |
| C.X与Y可能形成离子化合物XY |
| D.X与Y不可能形成共价化合物XY |
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:
2KClO3+H2C2O4+H2SO4
下列说法正确的是()
| A.KClO3在反应中被氧化为ClO2 |
| B.该反应的还原产物为CO2 |
| C.H2SO4在反应中是氧化剂 |
| D.0.5 mol H2C2O4参加反应有1 mol电子转移 |
在单质及共价化合物的晶体中,一定不存在()
| A.离子键 | B.共价键 |
| C.氢键 | D.分子间作用力 |
低碳经济要求减少煤、石油等消耗,减少二氧化碳排放。下列有关“低碳”的叙述不正确的是()
| A.可利用化工技术降低二氧化碳排放 |
| B.我国煤矿储量丰富,应大力发展火力发电 |
| C.为降低油耗,在飞机制造中采用具有特殊性能的碳纤维材料 |
| D.将二氧化碳注入蔬菜大棚作气体肥料 |