在2 L的密闭容器中,放入0.4 mol A和0.6 mol B,在一定温度下,压强为p,放入催化剂(体积忽略),发生反应2A(g)+3B(g)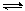 xC(g)+2D(g),在a min后,容器中c(A)=0. 1 mol·L-1,则a min内,v(B)=______ ______;若温度不变,压强变为0.9p,则v(C)=____ ___,x=_________。
xC(g)+2D(g),在a min后,容器中c(A)=0. 1 mol·L-1,则a min内,v(B)=______ ______;若温度不变,压强变为0.9p,则v(C)=____ ___,x=_________。
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________。
A. KMnO4 B. H2O2 C. Cl2水 D. HNO3
B. H2O2 C. Cl2水 D. HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。
A. NaOHB. NH3·H2OC. CuOD. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为_____ ___,
___, 通过计算确定上述方案________(填“可行”或“不可行”)。
通过计算确定上述方案________(填“可行”或“不可行”)。
在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=___________________。已知:K(300℃)>K(350℃),该反应是________热反应。
(2)右图中表示NO2的变化曲线是____________。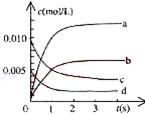
用O2表示从0~2s内该反应的平均速率v=___________。
(3)能说明该反应已经达到平衡状态的是___________。
a、v(NO2)=2v(O2) b、容器内压强保持不变
c、v逆(NO)=2v正(O2) d、容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a、及时分离出NO2气体 b、适当升高温度
c、增大O2的浓度 d、选择高效的催化剂
d、选择高效的催化剂
已知某溶液中只存在OH-、H+、NH 、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c(NH )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
②c(Cl-)>c(NH )>c(OH
)>c(OH -)>c(H+)
-)>c(H+)
③c(NH )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH )>c(OH-)
)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是_________,上述四种离子浓度的大小顺序为________(填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为_____________;若上述关系中④是正确的,则溶液中的溶质为____ ___。
(3) 若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系:c(H+)_______c(OH-)。
若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系:c(H+)_______c(OH-)。
(4)将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,则下面图像正确的是(填图像符号)________________;
已知:有机化合物A的分子式为C3H2O,能发生银镜反应。
回答下列问题:
(1)写出反应类型:反应①_________________反应②___________________。
(2)写出结构简式:A______________________ E。
(3)写出C8H8Cl2→E的化学方程式:____________________________________________
(4)物质C中共有14个碳原子,写出生成C的化学方程式_______________________。
(5)若C8H8Cl2苯环上的一溴取代物只有一种,其可能的结构除了外,还有和(用结构简式表示)。
蒽(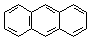 )与苯炔(
)与苯炔(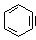 )反应生成化合物X(立体对称图形),如下图所示:
)反应生成化合物X(立体对称图形),如下图所示: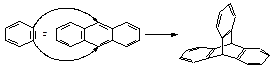
苯炔蒽 X
(1)蒽与X都属于____________。
a.环烃 b.烷烃 c.不饱和烃
(2)苯炔的分子式为________ _____,苯炔不具有的性质是_____________。
_____,苯炔不具有的性质是_____________。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)下列烃一定既能使溴水因反应褪色,又能使酸性高锰酸钾溶液褪色的是()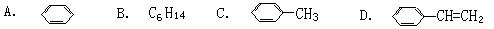
(4)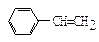 是生产某塑料的单体,写出合成该塑料的化学方程式:
是生产某塑料的单体,写出合成该塑料的化学方程式: