臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是______________和________________(填分子式)。
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示。已知:O3的起始浓度为0.0216 mol/L。
 pH pH t/min t/minT/℃ |
3.0 |
4.0 |
5.0 |
6.0 |
| 20 |
301 |
231 |
169 |
58 |
| 30 |
158 |
108 |
48 |
15 |
| 50 |
31 |
26 |
15 |
7 |
①pH增大能加速O3分解,表明对O3分解起催化作用的是________。
②在30 ℃、pH=4.0条件下,O3的分解速率为________mol/(L·min)。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为________(填字母代号)。
a.40 ℃、pH=3.0
b.10 ℃、pH=4.0
c.30 ℃、pH=7.0
可逆反应 ,在一定条件下达到平衡,若改变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:
,在一定条件下达到平衡,若改变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:
(1)升高温度,B转化率___________,v(正) ___________,v(逆)___________。
(2)使用催化剂,A的物质的量___________,若v(正)增大,则v(逆)____________。
(3)保持温度和压强不变加入稀有气体,则C的物质的量___________,A的转化率___________。
(4)保持温度和体积不变加入稀有气体,则A的转化率___________,v(正)_____________。
(5)若温度和体积不变,反应从正反应开始至平衡,在这个变化过程中,容器内气体的密度___________,压强___________。
反应A+3B=2C+2D在4种不同情况下的反应速率分别为:
该反应进行快慢的顺序为____________________.
(1)1.2g碳与适量水蒸气反应生成CO和H2,需吸收13. 128kJ热量,此反应的热化学方程式为_________________________________________。
常温下,取体积比4:1的甲烷和氢气的混合气体11.2 L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为____________。
已知X是一种具有果香味的合成香料,下图为合成X的某种流程: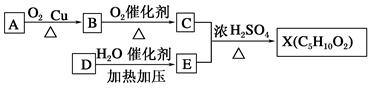
提示:① 不能最终被氧化为—COOH;
不能最终被氧化为—COOH;
②D的产量可以用来衡量一个国家的石油化工水平。
请根据以上信息,回答下列问题:
(1)A分子中官能团的名称是__________,X的结构简式是________。
(2)上述A、B、C、D、E、X六种物质中,互为同系物的是________________。
海水制取溴:
(1)主要流程: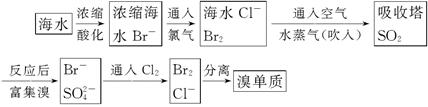
(2)主要反应(化学反应方程式):
_____________________________________。
(3)最后分离实验操作是、