为了比较①H-OH,②CH3COOH,③CH3CH2—OH,④H2CO3,⑤苯酚五种物质分子中—OH上氢原子的活动性顺序,某课外活动小组设计了如下表所示的实验方案。请你利用有关实验仪器及给出的试剂,填写表中的空格,完成上述实验方案。可供选用的试剂有:紫色石蕊试液、金属钠、氢氧化钠溶液、碳酸钠溶液。实验中所需仪器自选。
| 实验步骤和操作 |
实验现象 |
结论(-OH上氢原子活动性顺序) |
| (1).五种物质各取少量于五支试管中,各加入紫色石蕊试液2~3滴 |
②、④变红,其它不变 |
②、④>①、③、⑤ |
| (2). |
|
|
| (3).①、③、⑤各取少量于试管中,各加入少量NaOH溶液 |
⑤由浑浊变澄清 |
⑤>①、③ |
| (4). |
|
|
(5).通过以上实验比较,从而得出这五种物质分子中—OH上氢原子的活动性由强到弱的顺序为(填序号) 。
用图示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃)。已知:PCl3和PCl5遇水强烈反应,它们熔沸点数据如下: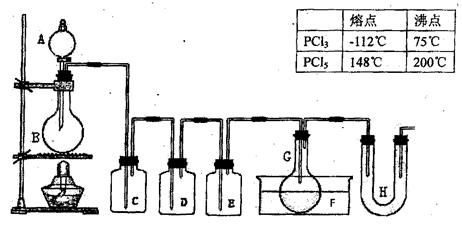
请根据图中装置回答下列问题:
(1)检查该装置气密性的方法是。
(2)为得到氯气,若B中加入MnO2,则A中应加入 ,发生反应的化学方程式为。
,发生反应的化学方程式为。
(3)若发现C中气泡产生过猛,需要进行的操作的关键是。
(4)在反应开始时主要生成PCl3,而后来主要生成PCl5,原因可能是;从PCl3和PCl5的混合物中分离也PCl3的最佳方法是(选填序号)。
a.蒸馏 b.分液 c.升华
(5)生成的PCl3在G中收集,则F中盛有,作用是
(6)C、D、H所盛的试剂分别是:C;D ;H。
;H。
(7)如果E中反应放热较多,G处的导管可能发生堵塞,其原因 是。
是。
(1)写出实验室由苯和浓硝酸反应制取硝基苯的化学方程式:.
该反应属于反应。
(2)如图所示的实验装置图中存在哪些错误?请指正。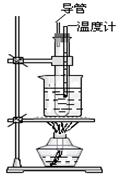
①;
②;
③。
(3)在试管中将两种浓酸混和的操作方法是
(4)试简述水浴加热的优点。
某学生用0.1 mol/L的KOH标准溶液滴定未知浓度盐酸,其操作分解为如下几步:
| A.移取20 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞 |
| B.用标准溶液润洗滴定管2~3次 |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3 cm |
E.调节液面至0或0以下刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空
(1)正确操作步骤的顺序是(用序号字母填写)____________________________;
(2)上述B步骤操作的目的是________________________________________________;
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果的影响是________;
(4)判断到达滴定终点的实验现象是_____________________________________;
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸则对滴定结果产生的影响是____________________________________。
 某探究
某探究 小组同学用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速率的因素。
小组同学用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速率的因素。
实验药品:2. 0moL/L 盐酸、4. 0mol/L盐酸、2 .0mol/L硫酸、4.0mol/L硫酸,质量和相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属
盐酸、4. 0mol/L盐酸、2 .0mol/L硫酸、4.0mol/L硫酸,质量和相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属 用量均为9. 0g。
用量均为9. 0g。
(Ⅰ)甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
| 反应进程(分钟) |
1 |
2 |
5 |
15 |
20 |
| 4.0mol/L盐酸 |
少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
反应结束 |
| 2.0mol/L硫酸 |
无明显现象 |
极少量气泡 |
少量气泡 |
||
| 4.0mol/L硫酸 |
无明显现象 |
少量气泡 |
有比 较连续的气泡 较连续的气泡 |
请回答:
(1)写出铝与盐酸反应的离子方程式。
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是
。
(3)以上探究铝与稀盐酸、稀硫酸反应速率有差异,你认为其原因有哪些可能?请提出 你的假设(写出2种可能):。
你的假设(写出2种可能):。
(Ⅱ)(1)乙同学设计了如下影响反应速率因素的实验(温度控制为25℃和35℃)。请你根据实验目的帮助该同学完成以下实验设计表(用量:酸均为50. 0mL、铝为9. 0g过量):
| 实验目的 |
实验 编号 |
温度 |
金属铝 形态 |
盐酸浓度 /mol·L-1 |
| 1. 实验①和②探究盐酸浓度对该反应速率的影响; 2. 实验①和③探究温度对该反应速率的影响; 3. 实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响。 |
① |
25˚ C C |
铝 |
4. 0 |
| ② |
||||
| ③ |
||||
| ④ |
某化学实验小组用如图所示的装置制取乙酸乙酯,并检验乙酸乙酯中是否含有乙酸杂质(铁架台、夹子等支撑仪器省略)。已知乙酸乙酯的沸点为77.1℃,乙醇沸点为78.4℃,乙酸的沸点为118℃。请根据要求填空:
⑴写出实验室用冰醋酸和无水乙醇制乙酸乙酯的化学方程式:
__________________。
⑵为使反应物充分反应,以下措施中正确的是(填写对应序号)。
①先小火温热,再慢慢升温至微沸状态②先大火加热至沸腾状态,并持续加热保持沸腾状态③使用稀硫酸作催化剂④作用浓硫酸作催化剂
⑶如果单孔塞上的导管短一些,对乙酸乙酯的收集有何影响,简述原因。
答:。
⑷A同学将收集到的乙酸乙酯滴入含有少量酚酞的NaOH溶液中并在水浴中温热,发现溶液的红色逐渐变浅,由此得出乙酸乙酯中含有乙酸的结论,你认为这一结论正确吗?为什么?
答:。
⑸B同学将收集到的乙酸乙酯滴入饱和NaHCO3溶液中,观察到有少量气泡产生,可得出的结论是,该过程中发生反应的化学方程式是。
⑹C同学将收集到的乙酸乙酯缓缓滴入饱和Na2CO3溶液中,无气泡产生,于是得出该乙酸乙酯中不含乙酸的结论。请你运用所学知识,评价该同学的结论是否正确。
我的评价是:。