右下图是以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
| 实验后的记录: ①Zn极发生还原反应,Cu极发生氧化反应 ②H+向负极移动 ③电子流动方向Zn→导线→Cu ④溶液的pH变小 ⑤若有1mol电子流过导线,则产生H2为0.5mol。 ⑥正极的电极反应式:Zn-2e- =Zn2+ |

(1)在卡片上,叙述合理的是___ __(填序号)。
(2)其他条件相同情况下,产生气泡的速率比单一锌片 (填快或慢)。
(3)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是___________________________。
(4)如果把硫酸换成硫酸铜溶液,猜测___(填“锌极”或“铜极”)变粗,原因是____ __(用电极方程式表示)。实验结束后称得两极质量差12.9g,假设初始时Zn极与Cu极质量相等,则反应中转移的电子的物质的量为 mol。
已知盐酸加到品红溶液中,由于酸性增强使品红溶液的红色加深。试推测:
(1)向品红溶液中通入过量SO2的过程中,观察到的现象为_________;
加热后的现象为________。
(2)向品红溶液中通入过量Cl2的过程中,观察到的现象为_________;
加热后的现象为_________。
(3)向品红溶液中通入物质的量之比为1∶1的SO2和Cl2后现象________。
(12分)A~G各物质间的关系如下图,其中B、D为气态单质。
MnO2①Fe点燃
MnO2②△
请回答下列问题:
(1)物质C和E的名称分别为________、________;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式___________;
若只能在加热情况下进行,则反应物A应为________;
(3)反应②的化学方程式为_____________________;
(4)新配制的F溶液应加入________以防止其转化为G。检验G溶液中阳离子的常用试剂
是________,实验现象为_____________________________。
硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用.试回答下列问题:
(1) 向大气中排放NOx可能导致的环境问题有.(答两点)已知足量NaOH溶液能完全吸收NO2生成氮的两种含氧酸盐(氮为+3、+5价).试写出该反应的离子方程式.
(2) 光导纤维的作用,让人们的生活更加丰富精彩,是制备光导纤维的基本原料.
(3) 氮化硅陶瓷是一种新型无机非金属材料,其化学式为,可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成,氮气在反应中既是反应物,同时又起了
作用.由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉.在烧结过程中,二氧化硅、碳、氮气以物质的量之比3∶6∶2反应生成两 种化合物,该反应的化学方程式为.
(4) 硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源.与“氢能源”比较“硅能源”具有等更加优越的特点,从而得到全球的关注和期待.
(1) 新制的氯水显色,这是因为氯水中有分子(填粒子符号)存在;向氯水中滴入几滴AgNO3溶液,观察到的现象是,说明氯水中有(填粒子符号)存在。紫色石蕊试液遇到氯水后,观察到的现象是;(2)工业用来制取漂白粉的反应方程式2Cl2+2Ca(OH)2= ;漂白粉露置在空气中久置变质失效的化学方程式为:、所以漂白粉应保存。
敌草胺是一种除草剂。它的合成路线如下: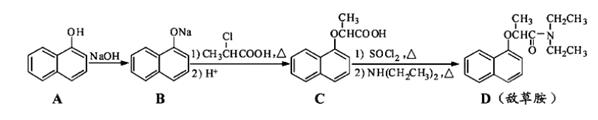
回答下列问题:
(1)在空气中久置,A由无色转变为棕色,其原因是。
(2)C分子中有2个含氧官能团,分别为和填官能团名称)。
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:。
①能与金属钠反应放出H2;②是萘(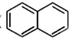 )的衍生物,且取代基都在同一个苯环上;
)的衍生物,且取代基都在同一个苯环上;
③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同
化学环境的氢。
(4)若C不经提纯,产物敌草胺中将混有少量副产物E(分子式为C23H18O3),E是一种酯。E的结构简式为。
(5)已知: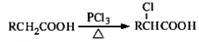 ,写出以苯酚和乙醇为原料制备
,写出以苯酚和乙醇为原料制备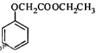 的合成路线流程图(无机试剂任用)。合成路线流程图例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图例如下: