1.28g铜和一定量的浓硝酸反应,
(1)若反应生成的气体全部为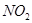 ,求消耗的
,求消耗的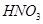 的物质的量。
的物质的量。
(2)若随着铜的不断减少,反应生成的气体的颜色也逐渐变浅。当铜全部反应时,共收集到标准状况下气体1.12L,求反应中消耗的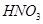 的物质的量。
的物质的量。
(8分)水在自然净化中要把有机污染物自发地转变为简单的无机物质,需要水中含有一定的氧气,使有机物(C,H,O)+O2 CO2+H2O。1 L水中含有的有机物转化为无机物所需要的氧的量称为生化需氧量(BOD),用g·L-1为单位表示。如果水中的氧气比BOD少,水就发臭,鱼和其他淡水生物就不能生存。若某地区一条河水中含有机物10 ppm(即质量分数为百万分之十),此有机物分子式用C6H10O5表示,而在正常大气条件下,氧气在水中的溶解量是0.009 2 g·L-1,水的密度为1 g·mL-1。
CO2+H2O。1 L水中含有的有机物转化为无机物所需要的氧的量称为生化需氧量(BOD),用g·L-1为单位表示。如果水中的氧气比BOD少,水就发臭,鱼和其他淡水生物就不能生存。若某地区一条河水中含有机物10 ppm(即质量分数为百万分之十),此有机物分子式用C6H10O5表示,而在正常大气条件下,氧气在水中的溶解量是0.009 2 g·L-1,水的密度为1 g·mL-1。
(1)写出有机物在有氧条件下转化为无机物的化学方程式。
(2)这条河水的BOD是多少?河水中的鱼类能否维持生命?
(1)分别写出相对分子质量为128、72的烃的分子式:__________、__________、__________。(可不写满,也可补充)
(2)立方烷的结构简式如图所示,每个顶点是一个碳原子。则: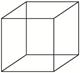
①其分子式为____________________。
②它的一氯取代物有__________种。
③它的二氯取代物有__________种。
(7分)某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20 min内平均速率为__________mol·L-1·min-1。
(2)在实验2,A的初始浓度为c2="__________" mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是_______________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3__________v1(填>、=或<),且c3__________1.0 mol·L-1(填>、=或<)。
(4)比较实验4和实验1,可推测该反应是__________反应(选填“吸热”或“放热”),理由是_____________________________________________________________________。
(11分)现将N2和H2在一定条件下合成氨。
(1)有一体积比为2∶3的N2和H2的混合气体,在一体积不变的密闭容器中发生反应,达到平衡时,容器内的压强为反应开始时的4/5,求:
①N2的转化率?
②平衡时n(N2)、n(H2)和n(NH3)的体积比是多少?
(2)在一定条件下,将一定量的N2和H2混合气体合成氨,达平衡时,混合气体中NH3的体积分数为25%。若反应前后条件相同,则反应从开始到平衡缩小的气体体积与原反应物气体体积的比值是多少?
在催化剂的作用下,乙炔可被氧化为乙二醛,进一步氧化,乙二醛又转化为乙二酸。某工厂生产乙二酸,每日可消耗乙炔气20.0 m3(已折算到标准状况),为监测产品质量,须不断抽样分析。假设某化验员抽取了10.00 g乙二酸产品,然后用6.00 mol·L-1的KOH(aq)进行滴定,达到滴定终点时消耗了碱液36.30 mL。求该工业乙二酸的纯度(已知乙二酸是强酸)。