下列各组物质中均有一种物质的类别与其他3种不同。
A.CaO,Na2O,CO2,CuO B.Si,C,P,Cu
C.O2,Fe,Cu,Zn D.HClO4,H2O,H2SO4,HNO3
(1)以上四组物质中类别不同的物质依次是 (填化学式)
A.________;B.____ ____;C.________;D.________。
(2)这四种物质相互作用可生成一种新物质碱式碳酸铜,化学式为Cu2(OH)2CO3,该化合物属于________(物质类别),该反应中________元素化合价变化(填“有”或“无”)。
对于下列氧化还原反应,请按要求填空。
(1)Cu + 4HNO3(浓)=== Cu(NO3)2 + 2NO2↑ + 2H2O
①氧化剂____________②离子方程式____________________________
(2)2H2S + SO2 === 3S↓ + 2H2O
①用双线桥法标出电子转移的方向和数目____________________________
②若氧化产物比还原产物多1.6g,则反应中电子转移的个数为________________
50 mL密度为1.84 g·cm-3,质量分数为98%的浓H2SO4,其H2SO4的物质的量浓度为。若将50 mL该浓H2SO4稀释成密度为1.47 g·cm-3的溶液100mL,需水mL。(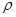 水=1g·cm-1)稀释后溶液的质量分数为,物质的量浓度为。
水=1g·cm-1)稀释后溶液的质量分数为,物质的量浓度为。
1.5molH2SO4的质量是_____________,其中含有__________mol H。
现有如下两个反应:
A、NaOH + HCl =" NaCl" + H2O
B、2FeCl3+Cu =2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池:A、, B、__________(选择“能”或“不能”);
(2)如果不能,说明其原因
________________________________________________________________;
(3)如果可以,则写出正、负极材料、电极反应式及电解质溶液名称:
负极材料________,电极反应式为,正极材料,电极反应式为,
电解质溶液名称是。
向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:
xA(g)+ yB(g) pC(g) + qD(g)。已知:平均反应速率V(C)=1/2V(A);反应2min时,A的浓度减少了1/3,B的物质的量减少了a/2mol,有amolD生成。回答下列问题:
pC(g) + qD(g)。已知:平均反应速率V(C)=1/2V(A);反应2min时,A的浓度减少了1/3,B的物质的量减少了a/2mol,有amolD生成。回答下列问题:
(1)反应2min内,A的平均反应速率是mol•L-1•min-1;
(2)原化学方程式中,化学计量数是:
A(g)+ B(g)  C(g) + D(g)
C(g) + D(g)
(3)反应平衡时,D为2amol,则B的转化率为;
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5amol,则该反应
的△H0;(填“>”、“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:
①反应速率增大,理由是体积减小,反应物的浓度增大,因而使反应速率增大;
②平衡时反应物的转化率(填“增大”、“减小”或“不变”),理由是