有一铁粉和氧化铜的混合物6.96g,进行如下实验: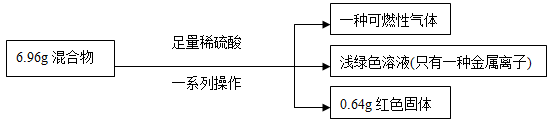
根据实验所得数据,关于混合物相关说法正确的是
| A.生成气体质量为0.2g |
| B.原混合物中铁的质量分数无法计算 |
| C.实验中反应的H2SO4质量为10.78g |
| D.原混合物中铜元素的质量不一定为0.64g |
下列物质的电子式书写正确的是
A.NaCl: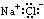 |
B.H2S: |
C.硫离子结构示意图: |
D.NH4I: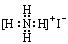 |
下列变化过程中,只破坏共价键的是
| A.I2升华 | B.NaF加热熔融 |
| C.HCl溶于水得盐酸 | D.蔗糖溶解 |
已知R2+有b个中子,核外有a个电子,表示R原子符号正确的是
2010年4月7日,俄罗斯科学家宣布在实验中获得了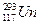 和
和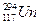 两种新原子。下列有关这两种原子的说法错误的是
两种新原子。下列有关这两种原子的说法错误的是
| A.质量数均超过质子数的两倍 | B.互称为同位素 |
| C.中子数分别为176、177 | D.是同一种核素 |
2009年6月5日是第三十八个世界环境日,该年度世界环境日的主题是:冰川消融,后果堪忧。在近百年间,全球平均气温升高了0.74℃,预计到本世纪末全球气温将升高1.1~6.4℃。下列做法可以减缓全球气温升高的是
①大力进行植树造林;②以煤等燃料为主要生活燃料;③鼓励私人购买和使用小汽车以代替公交车;④利用太阳能、风能和氢能新能源代替化石燃料;⑤禁止电动自行车上路
| A.①③④ | B.②⑤ | C.①④ | D.②③⑤ |