某研究性学习小组对某珍珠粉进行了如下探究。
【查阅资料】①珍珠的化学成分主要是:碳酸钙及少量碳酸镁和壳角蛋白(蛋白质的一种);
②壳角蛋白不溶于水,加入浓硝酸加热后会变黄色;
③假珍珠粉其实就是“贝壳粉”,主要成分就是碳酸钙。
【分析讨论】①真珍珠中所含壳角蛋白在物质类别上属于 (填 “有机”或“无机”)化合物。
②假珍珠粉中的碳酸钙含量要比真珍珠粉大。
【实验探究】研究性学习小组设计了如下两个方案:
方案一 检验珍珠粉的真假
取少量珍珠粉样品于试管中, ,若观察到 ,则该珍珠粉是真珍珠粉。
方案二 检验该珍珠粉中的碳酸钙含量
步骤Ⅰ:连接仪器组成如图所示实验装置。某学生夹住C左侧的橡胶管,在A中装入少量水并取下上部塞子,打开玻璃活塞,A中水不能全部滴下,你认为该装置是否漏气? 。
步骤Ⅱ:准确称取6.000 g珍珠粉样品装入仪器B中,在A中装入稀盐酸。
步骤Ⅲ:向B中珍珠粉样品中滴加足量的稀盐酸。在仪器B、C中可观察到的现象为 、 。
步骤Ⅳ:完全反应后C中的浊液经 、 、干燥,称得白色固体的质量为11.820g,则珍珠粉样品中碳酸钙的质量分数为100%。
【实验反思】获得此测定结果,可能的原因有 。(填数字序号)
①样品中含有碳酸镁
②盐酸未滴加足量
③CO2气流速度太快导致未被Ba(OH)2完全吸收
④装置B中水蒸气、HCl等进入装置C中
【拓展延伸】有同学提出在方案二中不需要装置C,只要用电子天平准确称量装置A、B反应前后的质量,就可以得到珍珠粉样品中碳酸钙的含量。你认为是否可行 ,请说明理由 。
一般情况下,金属越活泼,与酸反应速度越快。为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图所示):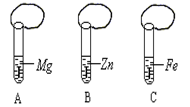
实验步骤:
①取A、B、C三支试管,分别加入2 mL浓度相同的盐酸溶液
②分别加入足量的、大小相等的Mg、Zn、Fe立即把三个相同
的气球分别套在各试管口上。实验预测与分析:
(1)写出锌与盐酸反应的化学方程式:_________________ ________。
(2)气球膨胀速度最快的是______________。(填试管编号)
(3)该实验表明,实验室一般用锌而不选用镁、铁制取氢气的主要原因是_。
(4)步骤②是实验获得成功的关键,你认为在操作过程中小组成员之间应该:________
(16分)小明知道二氧化锰能作过氧化氢分解的催化剂后,再想探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白。
(1)[问题]氧化铝能不能作过氧化氢分解的催化剂呢?
(2)[猜想]氧化铝能作过氧化氢分解的催化剂。
他设计并完成了下表所示的探究实验: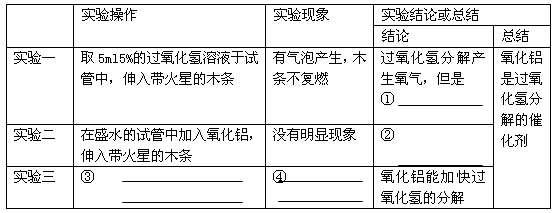
(1)请你帮助小明同学填写上表中未完的表格。
(2)在小明的探究实验中,实验一和实验二起的作用是______;
(3)[讨论与反思]经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充两个方面的探究实验,最终大家一起完成了对这个猜想的验证。
第一方面的实验操作中包含了两次称量,其目的是______
第二方面的实验是利用实验三反应后试管内的剩余物继续实验。接下来的实验操作是______现象和结论为______
元旦联欢会上,化学老师给同学们表演了一个“水能生火”的魔术(如图所示),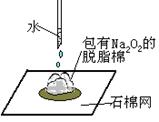
他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向棉花上滴了几滴水,棉花立刻燃烧了起来。同学们产生了浓厚的兴趣,为什么脱脂棉会燃烧起来呢?
【提出猜想】
a.小明认为过氧化钠(Na2O2)与水反应生成了可以支持燃烧的物质。
b.小刚又根据燃烧的条件,对小明的猜想进行了补充:。
【实验与分析】同学们设计了图的实验装置。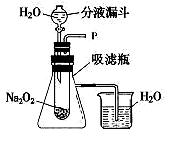
(1)打开分液漏斗的活塞,控制水滴加的速度,看到试管中有气泡产生,将带火星的木条靠近P出口,看到木条复燃,你推测此气体可能是。
(2)实验中还观察到,烧杯中的导气管口有气泡冒出,产生这一现象的原因是。
(3)完成了以上实验,老师介绍该反应的产物一共有两种,于是同学们又展开了进一步的研究,继续探究反应后生成的另一种物质。请你回答:另一种产物必含的元素是________,依据是_____________。
【老师介绍】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应,也能生成氧气。因此,过氧化钠经常被用于潜水艇和防毒面具中提供氧气。
【补充实验】
明确了以上性质,小芳同学又设计了一个实验(如图):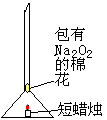
将一团包有过氧化钠的粉末的棉花塞到漏斗的管中,漏斗下方点燃一支短蜡烛 (蜡烛火焰与棉花不接触)。
请回答:
棉花 (填“能”或“不能”)燃烧。这主要是因为蜡烛燃烧生成能与过氧化钠(Na2O2)反应的物质___________________,同时反应放热。
物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变?
小刘、小李按下面的步骤进行探究:
(1)提出假设:物质发生化学变化前后总质量不变。
(2)设计并进行实验:小刘设计实验装置和选用药品如A所示,小李设计实验装置和选用药品如B所示,他们在反应前后都进行了规范操作、准确的称量和细致的观察。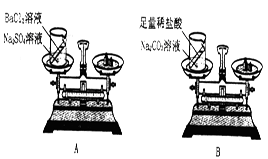
①这两个实验所发生的化学反应方程式为:
小刘的实验:BaCl2+Na2S04=BaS04↓+2NaCl
小李的实验:
②实验结论:
小刘认为:在化学反应中,生成物的总质量与反应物的总质量相等;
小李认为:在化学反应中,生成物总质量与反应物总质量不相等。
③你认为的结论正确,导致另一个实验结论错误的原因是:
④请从原子的角度分析你认为正确的结论的原因:
⑤使用上述实验装置,请你选择另外两种药品进行实验达到实验目的,这两种药品可以是(填化学式)[注:以上四种药品均不能再用]
(8分)小明设计了如下图所示的实验装置来证明氧化铜也能加快过氧化氢溶液的分解,并与相同条件下MnO2的催化效果做比较,实验时间均以生成30 mL气体为准(即比较反应的快慢程度)。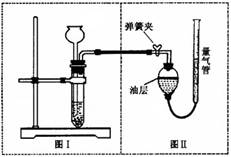
用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
| 实验序号 |
过氧化氢溶液体积 |
催化剂 |
待测数据 |
| ① |
15mL |
无 |
|
| ② |
15mL |
CuO(0.5g) |
|
| ③ |
15mL |
MnO2(0.5g) |
(1)检查图(Ⅰ)装置气密性的方法是:;
实验②操作时图(Ⅰ)装置中加入药品和试剂的先后顺序是,(用化学式填写);
(2)图(Ⅱ)装置中油层的作用是阻止氧气与水的接触,防止氧气。
(3)从设计原理看,实验中的“待测数据”是指。
(4)如果要进一步探究CuO是否是该反应的催化剂,根据催化剂的定义,请完成下列实验。
| 实验步骤和现象 |
设计这一步骤的目的 |
| (1)取15mL过氧化氢溶液,加入0.5g CuO后,产生O2的速率比未加入时快得多 |
CuO能加快过氧化氢溶液的分解 |