有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究。
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末。打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃。当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
【探究与反思】
打火石是 (填“混合物”或“纯净物”),这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧? ,这种蜡烛也可以熄灭,你采用的方法是 。
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
| 实验 |
操作步骤 |
现象 |
结论 |
| 1 |
切开蜡烛,取出打火石,用砂纸打磨 |
打火石是银白色 |
|
| 2 |
|
|
该金属一定不是铁 |
| 3 |
取少量打磨后的打火石于试管中,滴加硫酸铜溶液。 |
有红色物质析出 |
该金属一定是镁 |
【分析思考】
(1)请写出“实验3”中可能涉及到的化学方程式 。
(2)有同学认为通过“实验3”中现象不能证明烛芯内的金属一定是镁,
因为 。
(3)针对以上实验,请你设计一个合理的实验方案来进一步验证这种金属 。
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【查阅资料】电石主要成分为碳化钙(CaC2),它没有可燃性。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:;猜想三:Ca(OH)2。
他的依据是。
【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:
。
【进行实验】(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液,通入,有白色浑浊出现,证明猜想三成立。该反应的化学方程式为:。
结论:白色固体是Ca(OH)2。
【拓展应用】某市一辆满载电石的货车遇大雨引发熊熊大火,其中的可燃物是________,且该反应放出大量热,使可燃物达到_______________。
【交流反思】通过上述实验可知,电石在保存和运输时的注意事项_ ___
早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
(1)写出CO还原Fe2O3的化学方程式_____________________________。
(2)实验中盛澄清石灰水的试管中可观察到的现象是__________________。
(3)右边导气管口放置点燃的酒精灯的目的是__________________________。
(4)实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是__________________________________。
探究性学习小组的同学发现化学实验室一瓶块状固体已失去标签。科代表将固体取少量于试管中,加入足量的稀盐酸,有大量的气泡冒出,经检验气体密度大于空气,用向上排空气法收集到一集气瓶气体。同学们很兴奋,该固体可能是什么物质?他们设计实验方案,展开探究。
(1)猜想:产生的气体可能是___________。
(2)检验气体的实验记录如下:
| 实验操作 |
实验现象 |
结论 |
产生的气体是__________。 |
(3)根据上述实验结果推断,块状固体可能是____________________。
(4)实验室制取该气体的化学反应方程式是:。
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验。
| 实验编号 |
实验操作 |
实验现象 |
① |
分别在试管A、B中加入 5 mL 5%(溶液浓度) H2O2溶液,各滴入2 滴相同浓度的CuSO4溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 |
试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
| ② |
另取两支试管分别加入5mL 5%H2O2溶液和5 mL 10%H2O2溶液 |
试管A、B中均未明显见到有气泡产生。 |
(1)过氧化氢分解的化学方程式为。
(2)实验①的目的是。
实验中滴加CuSO4溶液的目的是。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你设计的实验方案是。(用实验中所提供的几种试剂)。
(4)对于H2O2分解反应,Fe2(SO4)3溶液也有一定的催化作用。为比较Fe2(SO4)3和CuSO4溶液对H2O2分解的催化效果。某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题: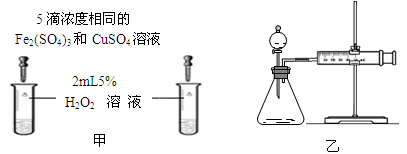
如图所示,同学们分别从定性和定量角度进行了比较。
①定性分析:如图甲可通过观察,定性比较得出结论。
②定量分析:用图乙所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是。
(5)通过对上述实验过程的分析,在实验设计时,要考虑________方法的应用。
(7分)实验室有一瓶试剂的标签破损不清如下图,
甲、乙、丙三位同学对它的主要成分进行讨论,一起猜想。
甲同学认为:该试剂主要成分是酸;
乙同学认为:该试剂主要成分是碱;
丙同学认为:该试剂主要成分是盐;
(1)你认为同学的猜想是错误的;
(2)丙同学证实该物质是一种氮肥,则化学式是;
(3)甲同学对有关盐的知识进行了以下的整理。
| 氯化钾 |
氯化钙 |
氯化钠 |
氯化镁 |
氯化铝 |
氯化锌 |
氯化亚铁 |
氯化铜 |
| KCl |
CaCl2 |
NaCl |
MgCl2 |
AlCl3 |
ZnCl2 |
FeCl2 |
CuCl2 |
反思:
①根据以上盐中的金属元素的排列,可以得出是依据顺序归纳整理的。
②酸在水溶液中能解离出H+,因此酸溶液具有相似的化学性质。据此分析上述盐溶液也会具有相似的化学性质,写出一种与上述盐溶液均能发生反应的物质的名称:。
(4)小组同学探究:除去固体氯化钠中混有的氯化钙。
设计实验方案如下,请参与实验并回答问题。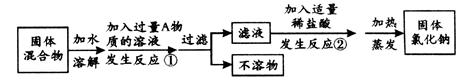
a.写出A物质的化学式:;
b.反应②中如果加入的稀盐酸也过量,则对所得到的氯化钠纯度(选填“有”或“没有”)影响;
c.分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果(选填“不变”、“增大”或“减小”)。