通过半年多时间的学习,同学们一定对下图装置很熟悉,请回答有关问题:
(1)写出标号仪器有名称:① ② ;
(2)我们知道有两种气体在实验室可以采用右图装置进行制取,请写出这两个制备反应的化学方程式 ; 。
现有一包久置的碱石灰干燥剂(主要成分CaO和NaOH),同学们用它进行了如下探究活动。
【猜想与假设】该干燥剂如果发生变质,则产物可能有(填一种)。
【实验与观察】
【解释与结论】白色沉淀a为,证明该干燥剂已经变质。由反应①可知b溶液中一定没有,反应②的化学方程式,b溶液中含有的溶质是。
【交流与反思】关于该干燥剂的保存或使用应注意
在实验室,同学们设计了如下装置制取纯净的二氧化碳。
【查阅资料】饱和碳酸氢钠溶液可以吸收HCI而不吸收CO2
(1)装置A中发生反应的化学方程式。
(2)装置C中AgNO3溶液的作用是,依据的原理是(用化学方程式表示),D装置中所盛药品是,若将C、D两装置中药品顺序颠倒,造成的后果是。
在实验室里,小珂同学看到氢氧化钠试剂瓶的瓶口有一层白色粉末。她对白色粉末的成分作出了一些猜测。
猜测一:可能是氢氧化钠
猜测二:可能是碳酸钠
猜测三:可能是氢氧化钠和碳酸钠
为探究白色粉末的成分,她将该粉末溶于水,得到无色溶液后,又进行了如下实验: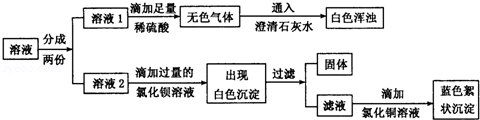
(1)根据实验现象推测,无色气体是。
(2)在溶液2中滴加过量氯化钡溶液的目的是。
(3)由实验现象可知,猜测是正确的。
二氧化硫(SO2)在通常情况下是一种无色、有刺激性气味的有毒气体,它能与氢氧化钠溶液反应生成盐与水。现有某探究实验小组欲利用如图装置和药品制取二氧化硫,并探究二氧化硫与水在通常情况下能否发生化学反应.设计的探究过程如下,请你回答其中的有关问题: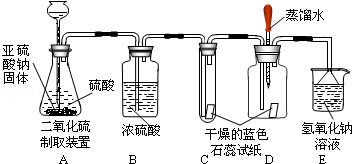
(1)假设:SO2与水在通常情况下能发生化学反应,生成物是一种酸.
(2)设计方案:先验证水能否使蓝色石蕊试纸变色;再验证SO2气体能否使干燥的蓝色石蕊试纸变色;最后验证SO2气体能否使湿润的蓝色石蕊试纸变红.
(3)查阅资料:你认为该研究小组需要查阅的资料内容中应包括下列中的(填写编号).
①SO2易溶于水,②酸能使湿润的蓝色石蕊试纸变红,③SO2能被浓硫酸干燥.
(4)实验:
①实验过程中,装置C内石蕊试纸的颜色始终没有变化,这说明.
②装置D中胶头滴管中的蒸馏水在SO2气体生成之前滴到蓝色石蕊试纸上,未见试纸颜色发生变化,当有SO2气体通过时,发现湿润的蓝色石蕊试纸变红,此现象说明.
③装置E的作用是,写出发生反应的化学方程式.
(5)结论:原假设(填“成立”“不成立”).
某中学化学课外活动小组在一次野外考察中,用三种不同的实验方法证实一口干枯的深井中二氧化碳的量很大.现请你完成实验报告:
| 实验方法 |
观察到的实验现象 |
解释实验现象 |
| (1)灯火实验 |
灯火 |
|
| (2)动物试验 |
动物 |
|
| (3)澄清石灰水试验 |
澄清石灰水 |
反应的化学方程式: |