有①甲烷,②乙烷,③丙烷,④丁烷4种烷烃,试回答下列问题:
(1)请写出烷烃(用通式表示)在足量的氧气中充分燃烧的化学方程式:
________________________________________________________________________。
(2)相同状况下,等体积的上述气态烃,消耗O2的量最多的是________ 。
(3)等质量的上述气态烃,在充分燃烧时,消耗O2的量最多的是________ 。
(4)存在同分异构体的是_______ _。
(5)在120 ℃,1.01×105Pa条件下,某气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃为________ 。
(6)10 mL某气态烃,在50 mL O2中充分燃烧,得到液态水,以及体积为35 mL的混合气体(所有气体体积均在同温同压下测定)。该气态烃是________ 。
在反应2KMnO4+16HCl 2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是,氧化产物是;若有1mol KMnO4参加反应时,该反应转移电子的个数是;若反应生成11.2LCl2(标准状况)则被氧化的氯化氢为mol;请在下面方框中用“单线桥法”表示该反应中电子转移的方向和数目。
2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是,氧化产物是;若有1mol KMnO4参加反应时,该反应转移电子的个数是;若反应生成11.2LCl2(标准状况)则被氧化的氯化氢为mol;请在下面方框中用“单线桥法”表示该反应中电子转移的方向和数目。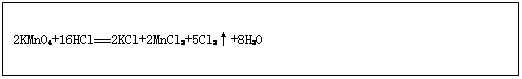
阅读下列材料后,回答相应问题。
一个体重50Kg的健康人大约含铁2g,这2g铁在人体中不是以单质金属形式存在,而是以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
(1)人体中经常进行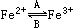 的相互转化,在A过程中,Fe2+做剂,在B过程中,Fe3+做剂。
的相互转化,在A过程中,Fe2+做剂,在B过程中,Fe3+做剂。
(2)“服用维生素C,可使食物中三价铁离子还原成二价铁离子。”这句话指出,维生素C在这一反应中做_剂,具有性。
(3)已知:氧化性Cl2> Br2> Fe3+, 还原性Fe2+>Br- >Cl-,则向0.2mol/L 1LFeBr2溶液中通入标准状况下氯气2.24L,被氧化的粒子是,此反应的离子方程式:。
离子反应方程式书写:(注意写化学方程式不给分)
(1)用盐酸中和烧碱,请写出其反应的离子方程式:
。
(2)用稀硫酸清洗铁锈(Fe2O3),请写出其反应的离子方程式:
。
(3)用足量的澄清石灰水检验二氧化碳,请写出其反应的离子方程式:
。
(4)小苏打能治疗胃酸(主要是盐酸)过多,请写出其反应的离子方
程式:。
(5)金属铝能与氢氧化钠溶液发生反应,请写出其反应的离子方程式:
。
(12分) 恒容密闭容器中,某化学反应2A  B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验序号 |
浓度(mol/L) |
时间(min) |
|||||||
| 0 |
10 |
20 |
30 |
40 |
50 |
60 |
|||
| 1 |
温 度 |
8000C |
1.0 |
0.80 |
O.64 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
8000C |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
| 3 |
8000C |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
| 4 |
8200C |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在前20min内用B的浓度变化来表示的平均速率
为mol/(L·min)。
(2)在实验2,A的初始浓度c2=mol/L,反应在 20分钟内就达到
平衡,可推测实验2中还隐含的条件是。
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1(用同种物质的浓度变
化表示),则达到平衡时υ3υ1(填>、=、<=)
且c3=mol/L。
(4)比较实验4和实验1,可推测该反应是反应(选填“吸热”、“放热”)。
(5) 800℃时,反应2A  B+D的平衡常数=,
B+D的平衡常数=,
实验2中达到平衡时A的转化率=。
20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
(1)图一是NO2和CO反应生成CO2和NO过程中能量变化示
意图,请写出NO2和CO反应的热化学方程式__________________________________
在反应体系中加入催化剂,E1和E2的变化是:E1_________,E2________(填“增大”、“减小”或“不变”),对反应热是否有影响?_______________,
原因是_
(2)图二是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程与能量关系图(图中的△H表示生成1mol产物的数据)。根据图二回答下列问题:
① PCl5(g)分解成PCl3(g)和Cl2(g)的热化学方程式
② P(s)和Cl2(g)分两步反应生成1molPCl5(g)的△H1与P(s)和Cl2(g)一步反应生成1molPCl5(g)
的△H2关系是:△H2______△H1(填“大于”、“小于”或“等于”),原因是
